题目内容
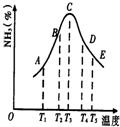 在容积不同的多个密闭容器内,分别充入同量的N2和H2,在不同温度下,同时发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图:
在容积不同的多个密闭容器内,分别充入同量的N2和H2,在不同温度下,同时发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图:(1)A,B,C,D,E五点中,尚未达到化学平衡状态的点是
(2)向一恒容容器中加入1mol N2和3mol H2,T3时,测得体系压强为原来的
| 7 | 8 |
(3)当上述反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3
产率的有
A 升高温度 B 降低温度 C 增大压强 D 减小压强
E 加入催化剂 F 吸收NH3 G 通入N2
(4)AC段的曲线和CE段曲线变化趋势相反,试从反应速率和平衡角度说明理由.
分析:(1)当NH3的体积分数最大时达到平衡状态,AB为氨气增大的阶段,不是平衡状态;DE是升高温度平衡逆移后的平衡状态;
(2)根据体系压强变化,求出参加反应的氮气的量,再根据热量求出反应热,写出热化学方程式;
(3)当上述反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3产率,即平衡正移,据此分析;
(4)AC段的曲线未达到平衡,CE段曲线达到平衡后升温平衡逆移;
(2)根据体系压强变化,求出参加反应的氮气的量,再根据热量求出反应热,写出热化学方程式;
(3)当上述反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3产率,即平衡正移,据此分析;
(4)AC段的曲线未达到平衡,CE段曲线达到平衡后升温平衡逆移;
解答:解:(1)当NH3的体积分数最大时达到平衡状态,AB为氨气增大的阶段,不是平衡状态;DE是升高温度平衡逆移后的平衡状态;故AB不是平衡状态,故答案为:AB;
(2)设参加反应的氮气为xmol
N2(g)+3H2(g)?2NH3(g)
起始量(mol) 1 3 0
变化量(mol) x 3x 2x
平衡量(mol) 1-x 3-3x 2x
容器内气体压强变为原来的
,即气体的物质的量变为原来的
,则
=
,则x=0.25
根据参加反应的物质的量之比等于放出的热量比,得:
=
,所以Q=92.4KJ,即1molN2参加反应放出热量为92.4KJ,所以其热化学方程式为:N2(g)+3H2 (g)═2NH3 (g)△H=-92.4 kJ/mol,
故答案为:N2(g)+3H2 (g)═2NH3 (g)△H=-92.4 kJ/mol;
(3)当上述反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3产率,即平衡正移;B 降低温度 C 增大压强 F 吸收NH3 G 通入N2 都看以使平衡正移,故BCFG正确,故答案为:BCFG;
(4)AC段的曲线反应开始时反应物浓度大,温度升高,反应速率增大,反应向正反应方向进行,生成NH3,氨气的浓度逐渐增大,CE段已经达到平衡,升高温度使平衡向逆反应方向移动,NH3%变小,
故答案为:AC段,反应开始时温度升高,反应速率增大,反应向正反应方向进行,生成NH3;CE段,已经达到平衡,升高温度使平衡向逆反应方向移动NH3%变小.
(2)设参加反应的氮气为xmol
N2(g)+3H2(g)?2NH3(g)
起始量(mol) 1 3 0
变化量(mol) x 3x 2x
平衡量(mol) 1-x 3-3x 2x
容器内气体压强变为原来的
| 7 |
| 8 |
| 7 |
| 8 |
| 1-x+3-3x+ 2x |
| 1+3 |
| 7 |
| 8 |
根据参加反应的物质的量之比等于放出的热量比,得:
| 1mol |
| 0.25mol |
| Q |
| 23.1kJ |
故答案为:N2(g)+3H2 (g)═2NH3 (g)△H=-92.4 kJ/mol;
(3)当上述反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3产率,即平衡正移;B 降低温度 C 增大压强 F 吸收NH3 G 通入N2 都看以使平衡正移,故BCFG正确,故答案为:BCFG;
(4)AC段的曲线反应开始时反应物浓度大,温度升高,反应速率增大,反应向正反应方向进行,生成NH3,氨气的浓度逐渐增大,CE段已经达到平衡,升高温度使平衡向逆反应方向移动,NH3%变小,
故答案为:AC段,反应开始时温度升高,反应速率增大,反应向正反应方向进行,生成NH3;CE段,已经达到平衡,升高温度使平衡向逆反应方向移动NH3%变小.
点评:本题考查了化学平衡的三部曲计算方法,影响化学平衡的因素等,题目难度中.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
(18分)在容积不同的多个密闭容器内,分别充入同量的N2和H2,在不同温度下,同时发生反应N2+3H2 2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如右:
2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如右:
(1)A,B,C,D,E五点中,尚未达到化学平衡状态的点是 。
(2) 向一恒容容器中加入1 mol N2 和3 mol H2,T3时,测得体系压强为原来的7/8,并放出23.1 kJ的热量,则该反应的热化学方程式为 。
(3)当上述反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高NH3产率的有 (填字母)
| A.升高温度 | B.降低温度 | C.增大压强 | D.减小压强 |
(4)AC段的曲线和CE段曲线变化趋势相反,试从反应速率和平衡角度说明理由。
。

 2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如右:
2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如右:
