题目内容
2.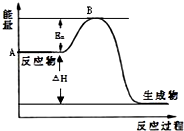 2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:
2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:(1)图中A点表示反应物的总能量,a=-198.
(2)Ea的大小对该反应的△H无(填“有”或“无”)影响.该反应常用V2O5作催化剂,加入V2O5会使图中B点降低(填“升高”、“降低”或“不变”).
(3)已知单质硫的燃烧热为296kJ•mol-1,写出反应的热化学方程式:S(s)+O2=SO2(g)△H=-296kJ•mol-1.
分析 (1)根据参加反应SO2的物质的量之比等于对应的△H之比;
(2)物质的活化能的大小与反应热无关;加入催化剂能降低物质的活化能;
(3)依据燃烧热的概念及热化学方程式的书写方法解答,燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量.
解答 解:(1)图象中A点为反应物的总能量,因1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1,所以2molSO2(g)氧化为2molSO3的△H=-198kJ•mol-1,则2SO2(g)+O2(g)=2SO3(g)△H=-198KJ•mol-1,
故答案为:反应物的总能量,-198;
(2)因物质的活化能的大小与反应热无关;加入催化剂能降低物质的活化能,则Ea降低,故答案为:无,降低;
(3)单质硫的燃烧热为296kJ•mol-1,因燃烧热概念要求必须是lmol物质完全燃烧,则热化学方程式为:S(s)+O2=SO2(g)△H=-296kJ•mol-1,
故答案为:S(s)+O2=SO2(g)△H=-296kJ•mol-1.
点评 本题考查反应过程的能量变化图以及运用盖斯定律进行反应热的计算,注意活化能与反应热的关系,注意燃烧热的定义,题目难度不大.

练习册系列答案
相关题目
12.下表为元素周期表的短周期部分.
请参照元素a-h在表中的位置,根据判断出的元素回答问题:
(1)h原子核外有4 种不同伸展方向的电子云,最外层共有7 种不同运动状态的电子.
(2)比较d、e元素常见离子的半径大小(用化学式表示)O2->Na+;b、c 两元素非金属性较强的是(写元素符号)N,写出证明这一结论的一个化学方程式2HNO3+Na2CO3 =2NaNO3+CO2↑+H2O.
(3)d、e元素形成的四原子化合物的电子式为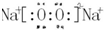 ;b、g元素形成的分子bg2为非极性分子(填写“极性”或“非极性”).
;b、g元素形成的分子bg2为非极性分子(填写“极性”或“非极性”).
上述元素可组成盐R:ca4f(gd4)2,和盐S:ca4agd4,
(4)相同条件下,0.1mol/L 盐R中c(ca4+)小于(填“等于”、“大于”或“小于”)0.1mol/L 盐S中c(ca4+).
(5)向盛有10mL1mol/L盐S溶液的烧杯中滴加1mol/L NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
(6)向盛有10mL 1mol/L盐 R溶液的烧杯中滴加1mol/L NaOH溶液32mL后,继续滴加至35mL写出此时段(32mL-35mL)间发生的离子方程式:NH4++OH-=NH3•H2O.若在10mL 1mol/L 盐R溶液的烧杯中加20mL1.2mol/L Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为0.022mol.
| a | |||||||
| b | c | d | |||||
| e | f | g | h |
(1)h原子核外有4 种不同伸展方向的电子云,最外层共有7 种不同运动状态的电子.
(2)比较d、e元素常见离子的半径大小(用化学式表示)O2->Na+;b、c 两元素非金属性较强的是(写元素符号)N,写出证明这一结论的一个化学方程式2HNO3+Na2CO3 =2NaNO3+CO2↑+H2O.
(3)d、e元素形成的四原子化合物的电子式为
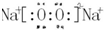 ;b、g元素形成的分子bg2为非极性分子(填写“极性”或“非极性”).
;b、g元素形成的分子bg2为非极性分子(填写“极性”或“非极性”).上述元素可组成盐R:ca4f(gd4)2,和盐S:ca4agd4,
(4)相同条件下,0.1mol/L 盐R中c(ca4+)小于(填“等于”、“大于”或“小于”)0.1mol/L 盐S中c(ca4+).
(5)向盛有10mL1mol/L盐S溶液的烧杯中滴加1mol/L NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
(6)向盛有10mL 1mol/L盐 R溶液的烧杯中滴加1mol/L NaOH溶液32mL后,继续滴加至35mL写出此时段(32mL-35mL)间发生的离子方程式:NH4++OH-=NH3•H2O.若在10mL 1mol/L 盐R溶液的烧杯中加20mL1.2mol/L Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为0.022mol.
13.下列物质不能通过化合反应或置换反应生成的是( )
| A. | Al2O3 | B. | HF | C. | Fe3O4 | D. | HClO |
17.在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是( )
| A. | 在含等物质的量的Ba(OH)2和KOH的混合溶液中,缓慢的通入足量CO2,反应先后顺序为Ba(OH)2、KOH、K2CO3、BaCO3 | |
| B. | 在含等物质的量的FeBr、FeI2溶液中,缓慢的通入氯气,离子反应发生的先后顺序为I-、Br-、Fe2+ | |
| C. | 在含等物质的量的NH4Cl、AlCl3溶液中,缓慢滴加NaOH溶液,先生成NH3•H2O后生成Al(OH)3沉淀 | |
| D. | 在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加盐酸,离子反应发生的先后顺序为AlO2-、OH-、CO32- |
7.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,22.4LSO3含有的分子数为NA | |
| B. | 常温常压下,17gNH3 所含的原子数目为4NA | |
| C. | 1 molCl2与H2O完全反应,转移2NA个电子 | |
| D. | 0.1mol/LNa2CO3溶液中含有的Na+数目为0.2NA |
14.对于胃溃疡较重的病人可使用的抑酸剂是( )
| A. | CaO | B. | Al(OH)3 | C. | NaHCO3 | D. | MgCO3 |
11.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 在透明的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | pH>7的溶液中:Fe2+、Cu2+、SO42-、Cl- | |
| C. | 有SO42-存在的溶液中:K+、Mg2+、Ag+、NO3- | |
| D. | 加入金属铝产生H2的溶液中:NH4+、Na+、SO42-、CH3COO- |
12.下列关于S、SO2、H2SO4的叙述中,正确的是( )
| A. | 硫是一种易溶于酒精的黄色晶体 | |
| B. | SO2溶于水生成H2SO4 | |
| C. | 可用氢氧化钠溶液处理含有SO2的尾气 | |
| D. | 浓H2SO4不稳定,光照易分解 |

 ;
;