题目内容
(8分)如图装置中,容器甲内充入1 mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体。恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时,容器体积缩小至最小,为原体积的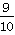 ,随着CO2的继续通入,活塞又逐渐向右移动(不考虑活塞的摩擦)
,随着CO2的继续通入,活塞又逐渐向右移动(不考虑活塞的摩擦)
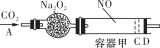
已知当活塞移至C处时,干燥管中物质的质量增加了22.4 g。
(1)当活塞移至C处时,通入标准状况下的CO2气体为_________________L。
(2)当活塞移至C处时,容器甲中NO2转化为N2O4的转化率是多少(注意:本小题要求写出计算过程)?
(3)活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至D处,则a值必_________0.1(填“大于”、“小于”或“等于”),其理由是_____________________________________.
(1) 17.92(2分) (2) 25%(2分)
(3)小于(2分); 其理由是活塞移至C,体积不会再减小,则干燥管中Na2O2已反应完,活塞由C向D移动,体积增大,2NO2 N2O4平衡将左移,使二者物质的量之和增多,活塞移至D时,气体物质的量共增加0.1mol,因此所需CO2必小于0.1mol(2分)。
N2O4平衡将左移,使二者物质的量之和增多,活塞移至D时,气体物质的量共增加0.1mol,因此所需CO2必小于0.1mol(2分)。
【解析】
试题分析:(1)设通入标准状况下CO2气体的体积为x,产生氧气的体积为y,
2Na2O2+2CO2 2Na2CO3+O2 Δm↑
2Na2CO3+O2 Δm↑
2×22.4 L 22.4 L 56 g
x y 22.4 g
解得x=17.92 L、y=8.96 L ,n(O2)=0.4 mol;
(2)由2NO + O2  2NO2知NO过量,生成NO2的物质的量为0.8 mol。
2NO2知NO过量,生成NO2的物质的量为0.8 mol。
所以2NO2 N2O4 Δn↓
N2O4 Δn↓
2 1 1
0.2 mol 1 mol×(1-9/10)=0.1mol
所以NO2转化为N2O4的转化率为0.2/0.8×100%=25%;
(3)活塞移至C,体积不会再减少,则干燥管中Na2O2已反应完,活塞由C向D移动,体积扩大,2NO2 N2O4平衡左移,使二者物质的量增多,活塞移至D时,气体物质的量共增加0.1 mol,因此所需CO2必小于0.1 mol。
N2O4平衡左移,使二者物质的量增多,活塞移至D时,气体物质的量共增加0.1 mol,因此所需CO2必小于0.1 mol。
考点:考查NO、CO2和过氧化钠反应的有关计算与判断、化学平衡。

 名校课堂系列答案
名校课堂系列答案(14分)工业上用闪锌矿(主要成分为ZnS,还含有Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:

(1)滤渣A经CS2提取后可获得一种淡黄色副产品,其化学式为 。
(2)浸取过程中Fe2(SO4)3的作用是 。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为 。该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是 。
(4)置换法除重金属离子所用物质C为 。
(5)硫酸锌的溶解度与温度之间的关系如下表:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
从除重金属后的硫酸锌溶液中获得硫酸锌晶体的实验操作为 、 、过滤、干燥。
 NH4++NH2-,其离子积常数为l.0xl0-30。现将2.3g金属钠投入1.0 L液氨中,则液氨电离平衡____ 移动(填“不”、“正方向”、“逆方向”);待反应结束后,假设溶液的体积不变,所得溶液中NH4+的浓度为____ 。
NH4++NH2-,其离子积常数为l.0xl0-30。现将2.3g金属钠投入1.0 L液氨中,则液氨电离平衡____ 移动(填“不”、“正方向”、“逆方向”);待反应结束后,假设溶液的体积不变,所得溶液中NH4+的浓度为____ 。


 )在催化剂作用下也能生成化合物Ⅱ,同时得到一种副产品G,下列有关G的说法正确的是 。
)在催化剂作用下也能生成化合物Ⅱ,同时得到一种副产品G,下列有关G的说法正确的是 。  ),H的同分异构体有多种,请写出符合下列条件的H的一种同分异构体 。
),H的同分异构体有多种,请写出符合下列条件的H的一种同分异构体 。

 H++A2-
H++A2-