题目内容
1.下列有关化学键的叙述,正确的是( )| A. | 离子化合物中不可能含有共价键 | |
| B. | 非金属单质分子中一定存在共价键 | |
| C. | 离子化合物中不一定含有离子键 | |
| D. | 含有共价键的化合物不一定是共价化合物 |
分析 A、离子化合物中可能含有共价键;
B、单原子分子构成非金属单质不含化学键;
C、离子化合物中一定含离子键,可能含共价键;
D、离子化合物中一定含离子键,可能含共价键.
解答 解:A、离子化合物中可能含有共价键,如NaOH等,故A错误;
B、非金属单质不一定存在共价键,如:稀有气体中不存在化学键,故B错误;
C、离子化合物中一定含有离子键,故C错误;
D、含有共价键的化合物不一定是共价化合物,如NaOH,故D正确;
故选D.
点评 本题考查了离子键、共价键与离子化合物、共价化合物的关系,要注意的是:离子化合物中可能含共价键,共价化合物中一定不含离子键.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
11.下列说法正确的是( )
| A. | 有机物CH2Cl-CH2Cl用系统命名法命名为:二氯乙烷 | |
| B. | 1mol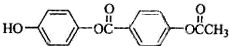 与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol 与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol | |
| C. | 标准状况下,22.4L己烷所含分子数为NA | |
| D. | 乙醇与乙酸发生酯化反应时,乙醇分子中的碳氧键没断裂 |
16.用VSEPR模型预测下列分子或离子的立体结构,其中正确的是( )
| A. | CS2为V形 | B. | HCN为V形 | ||
| C. | NH${\;}_{4}^{+}$为正四面体形 | D. | PCl3为平面三角形 |
6.下列说法正确的是( )
| A. | 22.4L N2的物质的量为1mol | |
| B. | 标准状况下,1mol任何物质的体积为22.4L | |
| C. | SO2的摩尔质量与相对分子质量相等 | |
| D. | 在相同温度、压强下,相同体积的任何气体分子数相同 |
13.下列有关叙述中不正确的是( )
| A. | 只用试管和胶头滴管就可区分纯碱溶液和稀盐酸 | |
| B. | Fe(OH)3是难溶于水的碱,但能通过化合反应生成 | |
| C. | 在FeCl3溶液中加入足量Cu充分反应后,溶液中的溶质只有CuCl2 | |
| D. | 有Al2O3制取Al(OH)3的途径如下图,则X可能是NaOH,也可能是HCl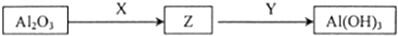 |
10.已知某元素的化合价为+7价,下列说法中正确的是( )
| A. | 该元素在元素周期表中一定处于ⅦA族 | |
| B. | 该元素可能是氟元素 | |
| C. | 该元素的某种化合物可能具有漂白性 | |
| D. | 该元素的单质一定是非金属 |
11.下列说法不正确的是( )
| A. | 实验室用Ca(OH)2固体和NH4Cl固体共热制NH3 | |
| B. | 常温下铁遇浓硝酸钝化,常温下可用铁罐储存浓硝酸 | |
| C. | 向蔗糖中滴入浓硫酸后变黑,体现了浓硫酸的脱水性 | |
| D. | FeCl2溶液中滴入KSCN溶液,溶液变红 |