��Ŀ����
������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����ش��������⣺
��1����֪C��s��+H2O��g��?CO��g��+H2��g������÷�Ӧ��ƽ�ⳣ������ʽΪ ��
��2����֪��һ���¶��£�
C��s��+CO2��g��?2CO��g����H1
CO��g��+H2O��g��?H2��g��+CO2��g����H2
C��s��+H2O��g��?CO��g��+H2��g����H3
���H1����H2����H3֮��Ĺ�ϵ�ǣ� ��
��3��ͨ���о���ͬ�¶���ƽ�ⳣ�����Խ��ijЩʵ�����⣮��֪�������һ����̼��ˮ�������뷴Ӧʱ���ᷢ�����·�Ӧ��CO��g��+H2O��g��?H2��g��+CO2��g�����÷�Ӧƽ�ⳣ�����¶ȵı仯�����ʾ��
��÷�Ӧ������Ӧ������ ��Ӧ������ȡ����ȡ�������500��ʱ��������ʼʱCO��H2O����ʼŨ�Ⱦ�Ϊ0.020mol/L����CO��ƽ��ת����Ϊ ��
��4���Ӱ����������������ᣬ�˹������漰���������NO��NO2��N2O4�ȣ��Է�ӦN2O4��g��?2NO2��g����H��0���¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ1��ʾ������˵����ȷ���� ��

A��A��C����ķ�Ӧ���ʣ�A��C
B��A��C�����������ɫ��A�Cdz
C��B��C����������ƽ����Է���������B��C
D����״̬A��״̬B�������ü��ȵķ���
E��A��C����Ļ�ѧƽ�ⳣ����A=C
��5����ҵ����Na2SO3����β���е�SO2������ͼ2װ�õ�⣨���Ե缫��NaHSO3��ȡH2SO4�������ӽ���Ĥֻ����������ͨ�����������缫��ӦʽΪ�� ���������ݳ�����ijɷ�Ϊ ���ѧʽ����
��1����֪C��s��+H2O��g��?CO��g��+H2��g������÷�Ӧ��ƽ�ⳣ������ʽΪ
��2����֪��һ���¶��£�
C��s��+CO2��g��?2CO��g����H1
CO��g��+H2O��g��?H2��g��+CO2��g����H2
C��s��+H2O��g��?CO��g��+H2��g����H3
���H1����H2����H3֮��Ĺ�ϵ�ǣ�
��3��ͨ���о���ͬ�¶���ƽ�ⳣ�����Խ��ijЩʵ�����⣮��֪�������һ����̼��ˮ�������뷴Ӧʱ���ᷢ�����·�Ӧ��CO��g��+H2O��g��?H2��g��+CO2��g�����÷�Ӧƽ�ⳣ�����¶ȵı仯�����ʾ��
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
��4���Ӱ����������������ᣬ�˹������漰���������NO��NO2��N2O4�ȣ��Է�ӦN2O4��g��?2NO2��g����H��0���¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ1��ʾ������˵����ȷ����

A��A��C����ķ�Ӧ���ʣ�A��C
B��A��C�����������ɫ��A�Cdz
C��B��C����������ƽ����Է���������B��C
D����״̬A��״̬B�������ü��ȵķ���
E��A��C����Ļ�ѧƽ�ⳣ����A=C
��5����ҵ����Na2SO3����β���е�SO2������ͼ2װ�õ�⣨���Ե缫��NaHSO3��ȡH2SO4�������ӽ���Ĥֻ����������ͨ�����������缫��ӦʽΪ��
���㣺�ø�˹���ɽ����йط�Ӧ�ȵļ���,����İٷֺ�����Ũ�ȡ�ʱ��ı仯����,��ѧƽ��ļ���,���ԭ��
ר�⣺�����������������
��������1��ƽ�ⳣ������ʽ��дע�⣬���ù�̬�ʹ�Һ�壻
��2�����ݸ�˹���ɽ��
��3�������¶ȱ仯ƽ�ⳣ���ı仯�ж��¶ȶԻ�ѧƽ���ƶ���Ӱ�죬�����жϷ�Ӧ�ȣ���������ʽ������ת���ʣ�
��4����ƽ���ƶ��ĽǶȷ������������ı仯
��5�����ݵ��ԭ�������������������Ӧ������������ԭ��Ӧ���Դ���д�缫��Ӧʽ��
��2�����ݸ�˹���ɽ��
��3�������¶ȱ仯ƽ�ⳣ���ı仯�ж��¶ȶԻ�ѧƽ���ƶ���Ӱ�죬�����жϷ�Ӧ�ȣ���������ʽ������ת���ʣ�
��4����ƽ���ƶ��ĽǶȷ������������ı仯
��5�����ݵ��ԭ�������������������Ӧ������������ԭ��Ӧ���Դ���д�缫��Ӧʽ��
���
�⣺��1����ӦC��s��+H2O��g��?CO��g��+H2��g����CΪ���壬������ƽ�ⳣ������ʽΪ��K=
��
�ʴ�Ϊ��K=
��
��2����֪��
��C��s��+CO2��g��?2CO��g����H1
��CO��g��+H2O��g��?H2��g��+CO2��g����H2
��C��s��+H2O��g��?CO��g��+H2��g����H3
�ݸ�˹���ɣ���+��=�ۣ�
�ʴ�Ϊ����H3=��H1+��H2���H1=��H3-��H2���H2=��H3-��H1��
��3���ɱ������ݿ�֪�������¶ȵ����ߣ�ƽ�ⳣ����С��˵�������¶�ƽ�����淴Ӧ�����ƶ���˵������ӦΪf���ȷ�Ӧ����ת����COŨ��Ϊx��
CO��g��+H2O��g��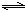 H2��g��+CO2��g����
H2��g��+CO2��g����
��ʼ��mol/L�� 0.020 0.020 0 0
ת����mol/L�� x x x x
ƽ�⣨mol/L����0.02-x����0.02-x�� x x
����
=9
��֮�ã�x=0.015mol/L��
����ת����Ϊ��
��100%=75%��
�ʴ�Ϊ�����ȣ�75%��
��4���Է�ӦN2O4��g��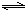 2NO2��g������H��0�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ2��ʾ����
2NO2��g������H��0�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ2��ʾ����
A��A��C�����¶���ͬ��A��ѹǿС��C���ѹǿ��ѹǿԽ��Ӧ����Խ����Ӧ���ʣ�A��C����A����
B��һ���棬����ѹǿ��N2O4��NO2��Ũ�ȶ����ӣ���һ���棬�÷�Ӧ�������������ķ�Ӧ������ѹǿ��ƽ�������ƶ���NO2�ٷֺ������ͣ���ƽ����ƶ����ܵ���Ũ�ȵ����ӣ�����NO2Ũ�����������A�㣬C����ɫ�����B����
C��B��C����������������������ͬ�����������ƽ����Է���������ͬ����C����
D��A��B����ѹǿ��ͬ���÷�Ӧ�����ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ�������������������������D����
E��A��C�����¶���ͬ����ѧƽ�ⳣ����ͬ����E��ȷ��
�ʴ�Ϊ��E��
��5�����NaHSO3��Һ��ȡH2SO4�������������ӷŵ磬���ں�������Ļ�ԭ�Ա�����������ǿ�����������������������ӷŵ磬����������������ӻ�������ӷ�Ӧ���ɶ����������壮
�ʴ�Ϊ��HSO3-+H2O-2e-=SO42-+3H+��O2��SO2��
| c(CO)��c(H2) |
| c(H2O) |
�ʴ�Ϊ��K=
| c(CO)��c(H2) |
| c(H2O) |
��2����֪��
��C��s��+CO2��g��?2CO��g����H1
��CO��g��+H2O��g��?H2��g��+CO2��g����H2
��C��s��+H2O��g��?CO��g��+H2��g����H3
�ݸ�˹���ɣ���+��=�ۣ�
�ʴ�Ϊ����H3=��H1+��H2���H1=��H3-��H2���H2=��H3-��H1��
��3���ɱ������ݿ�֪�������¶ȵ����ߣ�ƽ�ⳣ����С��˵�������¶�ƽ�����淴Ӧ�����ƶ���˵������ӦΪf���ȷ�Ӧ����ת����COŨ��Ϊx��
CO��g��+H2O��g��
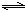 H2��g��+CO2��g����
H2��g��+CO2��g������ʼ��mol/L�� 0.020 0.020 0 0
ת����mol/L�� x x x x
ƽ�⣨mol/L����0.02-x����0.02-x�� x x
����
| x��x |
| (0.02-x)��(0.02-x) |
��֮�ã�x=0.015mol/L��
����ת����Ϊ��
| 0.015mol/L |
| 0.02mol/L |
�ʴ�Ϊ�����ȣ�75%��
��4���Է�ӦN2O4��g��
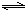 2NO2��g������H��0�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ2��ʾ����
2NO2��g������H��0�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ2��ʾ����A��A��C�����¶���ͬ��A��ѹǿС��C���ѹǿ��ѹǿԽ��Ӧ����Խ����Ӧ���ʣ�A��C����A����
B��һ���棬����ѹǿ��N2O4��NO2��Ũ�ȶ����ӣ���һ���棬�÷�Ӧ�������������ķ�Ӧ������ѹǿ��ƽ�������ƶ���NO2�ٷֺ������ͣ���ƽ����ƶ����ܵ���Ũ�ȵ����ӣ�����NO2Ũ�����������A�㣬C����ɫ�����B����
C��B��C����������������������ͬ�����������ƽ����Է���������ͬ����C����
D��A��B����ѹǿ��ͬ���÷�Ӧ�����ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ�������������������������D����
E��A��C�����¶���ͬ����ѧƽ�ⳣ����ͬ����E��ȷ��
�ʴ�Ϊ��E��
��5�����NaHSO3��Һ��ȡH2SO4�������������ӷŵ磬���ں�������Ļ�ԭ�Ա�����������ǿ�����������������������ӷŵ磬����������������ӻ�������ӷ�Ӧ���ɶ����������壮
�ʴ�Ϊ��HSO3-+H2O-2e-=SO42-+3H+��O2��SO2��
���������⿼���Ϊ�ۺϣ��漰֪ʶ��϶࣬�ѶȽϴ��״���Ϊ��5����

��ϰ��ϵ�д�
 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�
�����Ŀ
��ǿ������Һ�У����и������ӿ�������������ԭ��Ӧ�����ܴ���������ǣ�������
| A��Na+��K+��SO42-��Cl- |
| B��Na+��ClO-��SO42-��Fe2+ |
| C��Ba2+��K+��HCO3-��NO3- |
| D��Ba2+��Na+��SO42-��AlO2- |
���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
| A�������ۼ���ϡ�����У�2Fe+6H+=2Fe3++3H2�� |
| B�������м���̼��ƣ�CO32-+2H+�TH2O+CO2�� |
| C��ͭƬ�������Ȼ�����Һ�У�Cu+2Fe3+�T2Fe2++Cu2+ |
| D��NaHCO3��Һ��NaOH��Һ��Ӧ��OH-+HCO3-=CO32-+H2O |
���и������У�����˳���칹����ǣ�������
| A��1-��ϩ | B����ϩ |
| C��2-��-2-��ϩ | D��2-��ϩ |
 ����ͼ��ʾװ���ռ�����8�����壨ͼ����ƿ��λ�ò��ñ仯����
����ͼ��ʾװ���ռ�����8�����壨ͼ����ƿ��λ�ò��ñ仯���� �����̲��Ŵ����ġ���ȼ�������ü�����ˮú����CO��H2�����ٺϳɼ״����������湩Ӧ���ŵ�ȼ�ͣ�
�����̲��Ŵ����ġ���ȼ�������ü�����ˮú����CO��H2�����ٺϳɼ״����������湩Ӧ���ŵ�ȼ�ͣ� ��ͼΪ��ѧ�������ʼ��ת����ϵ�����мס��ҡ�������Ϊ���ʣ�����Ϊ�������������Ԫ������������������������C������Ϊ��ɫҺ�壬B��ɫ��ӦΪ��ɫ��һЩ����Һ�н��еķ�Ӧ��Һ�е�H2O�����ɵ�H2O��ʡ�ԣ��ش��������⣺
��ͼΪ��ѧ�������ʼ��ת����ϵ�����мס��ҡ�������Ϊ���ʣ�����Ϊ�������������Ԫ������������������������C������Ϊ��ɫҺ�壬B��ɫ��ӦΪ��ɫ��һЩ����Һ�н��еķ�Ӧ��Һ�е�H2O�����ɵ�H2O��ʡ�ԣ��ش��������⣺