题目内容
下列说法正确的是( )
| A、常温下可用铝制容器贮存稀硝酸 |
| B、钠的化学性质活泼,可从CuSO4溶液中置换出Cu |
| C、干燥的氯气具有漂白性 |
| D、金属钠与氧气反应,条件不同产物不同 |
考点:铝的化学性质,氯气的化学性质,钠的化学性质
专题:
分析:A、铝与冷的浓硝酸发生钝化,和稀硝酸要发生氧化还原反应;
B、钠与水反应生成氢氧化钠,氢氧化钠与CuSO4溶液复分解生成氢氧化铜;
C、燥的氯气无漂白性,只有湿润的氯气与水反应生成次氯酸的强氧化性漂白;
D、金属钠与氧气反应,如果在暴露的空气中表面变暗生成氧化钠,若在氧气中点燃生成过氧化钠.
B、钠与水反应生成氢氧化钠,氢氧化钠与CuSO4溶液复分解生成氢氧化铜;
C、燥的氯气无漂白性,只有湿润的氯气与水反应生成次氯酸的强氧化性漂白;
D、金属钠与氧气反应,如果在暴露的空气中表面变暗生成氧化钠,若在氧气中点燃生成过氧化钠.
解答:
解:A、铝与冷的浓硝酸发生钝化,和稀硝酸要发生氧化还原反应,所以常温下不可用铝制容器贮存稀硝酸,故A错误;
B、钠与水反应生成氢氧化钠,氢氧化钠与CuSO4溶液复分解生成氢氧化铜,得不到铜单质,故B错误;
C、燥的氯气无漂白性,只有湿润的氯气与水反应生成次氯酸的强氧化性漂白,故C错误;
D、金属钠与氧气反应,如果在暴露的空气中表面变暗生成氧化钠,若在氧气中点燃生成过氧化钠,所以条件不同产物不同,故D正确;
故选D.
B、钠与水反应生成氢氧化钠,氢氧化钠与CuSO4溶液复分解生成氢氧化铜,得不到铜单质,故B错误;
C、燥的氯气无漂白性,只有湿润的氯气与水反应生成次氯酸的强氧化性漂白,故C错误;
D、金属钠与氧气反应,如果在暴露的空气中表面变暗生成氧化钠,若在氧气中点燃生成过氧化钠,所以条件不同产物不同,故D正确;
故选D.
点评:本题考查铝、硝酸、钠和次氯酸的漂白性等知识,侧重于基础知识的考查,注意钠与盐溶液反应的情况,难度不大.

练习册系列答案
相关题目
现用pH=3的CH3COOH溶液和pH=11的NaOH溶液各V mL,进行中和滴定,当滴定到pH=7时,锥形瓶内溶液的体积为(滴定前后溶液未稀释、总体积不变)( )
| A、等于2V mL |
| B、小于2V mL |
| C、大于2V mL |
| D、无法确定 |
下列行为中,符合安全要求的是( )
| A、金属钠意外着火时,立即用沾水的毛巾覆盖 |
| B、当有大量氯气泄漏时,人应沿顺风方向疏散 |
| C、将含有硫酸的废液倒入水池,用大量水冲入下水道 |
| D、严禁在加油站附近放烟花爆竹 |
下列说法正确的是( )
| A、绿色食品是不含任何化学物质的食品 |
| B、Na2O2与CO2反应,Na2O2是氧化剂、CO2是还原剂 |
| C、与同浓度的硫酸反应时,NaHCO3比Na2CO3剧烈 |
| D、称取等质量的两份铝粉,分别加入过量的稀盐酸和过量的NaOH溶液,则放出氢气的体积(同温同压下)不相等 |
下列化合物的核磁共振氢谱中出现三个峰的是( )
| A、2,5二甲基己烷 |
| B、3,4二甲基己烷 |
| C、2,3,4三甲基戊烷 |
| D、2,2,3,3四甲基丁烷 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、使甲基橙变红色的溶液:Na+、Mg2+、Cl-、SO42- |
| B、0.1mol?L-1 NaHCO3溶液:Na+、Ba2+、NO3-、OH- |
| C、滴加KSCN 溶液显红色的溶液:NH4+、K+、Cl-、I- |
| D、由水电离出的c(H+)=10-12mol?L-1的溶液:Na+、K+、NO3-、ClO- |
 下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.
下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.
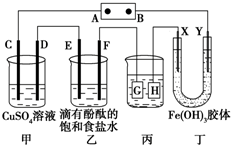 如图所示装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中的溶液都是1mol?L-1 500mL(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答:
如图所示装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中的溶液都是1mol?L-1 500mL(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答: