题目内容
(10分)工业上用CO生产燃料甲醇,一定条件下发生反应: CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
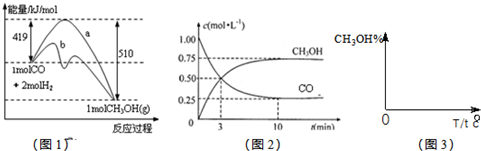
(1)图1是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)= 。
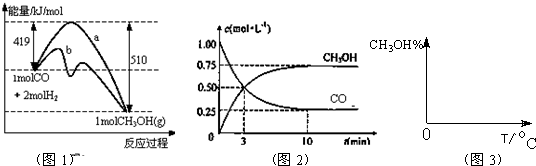
(2)图2表示该反应进行过程中能量的变化。曲线 (填“a”或“b”)表示不使用催化剂时反应的能量变化,不使用催化剂时该反应的逆反应的活化能为 。
(3)该反应平衡常数K的表达式为 ,温度升高,平衡常数K (填“增 大”、“不变”或“减小”)
大”、“不变”或“减小”)
(4)恒容条件下,下列措施中能使 增大的有 。
增大的有 。
| A.升高温度 | B.充入He气 |
| C.再充入1molCO和2molH2 | D.使用催化剂 |
(1)0.075mol/(L·min)(2分) (2)a(1分) 510kJ/mol(2分)
(3) (1分) 减小(2分)(4)C(2分)
(1分) 减小(2分)(4)C(2分)
解析

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目


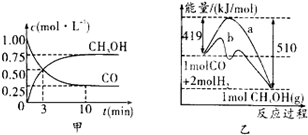
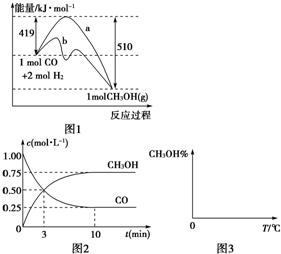 工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.
工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.