题目内容
 在恒容条件下发生反应A(g)+3B(g)
在恒容条件下发生反应A(g)+3B(g)| 催化剂 |
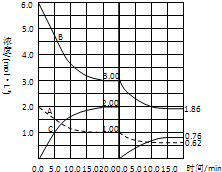
改变其他反应条件,在Ⅰ、Ⅱ阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法中正确的是( )
| A、第Ⅰ阶段用C表示的平衡前的反应速率v (C)=0.1 mol/(L?S) |
| B、第Ⅱ阶段中B的平衡转化率αⅡ(B)为0.019 |
| C、第Ⅰ阶段的平衡常数KⅠ与第Ⅱ阶段平衡常数KⅡ的大小关系是:KⅠ<KⅡ |
| D、由第一次平衡到第二次平衡,可能采取的措施是从反应体系中移出产物C |
分析:A.由图可知,第Ⅰ阶段20min到达平衡,平衡时△c(C)=2mol/L,根据v=
计算v(C);
B.由图可知,第Ⅱ阶段平衡时△c(B)=3mol/L-1.86mol/L=1.14mol/L,转化率是物质的减少量与初始量的比值,据此计算;
C.第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡常数只受温度影响;
D.第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度.
| △c |
| △t |
B.由图可知,第Ⅱ阶段平衡时△c(B)=3mol/L-1.86mol/L=1.14mol/L,转化率是物质的减少量与初始量的比值,据此计算;
C.第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡常数只受温度影响;
D.第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度.
解答:解:A.由图可知,第Ⅰ阶段20min到达平衡,平衡时△c(C)=2mol/L,故v(C)=
=0.1mol/(L?min),故A错误;
B.由图可知,第Ⅱ阶段平衡时△c(B)=3mol/L-1.86mol/L=1.14mol/L,故第Ⅱ阶段中B的平衡转化率αⅡ(B)=
×100%=38%,故B错误;
C.第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡常数只受温度影响,第Ⅰ阶段与第Ⅱ阶段的温度相同,故平衡常数KⅠ=KⅡ,故C错误;
D.第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,故D正确;
故选D.
| 2mol/L |
| 20min |
B.由图可知,第Ⅱ阶段平衡时△c(B)=3mol/L-1.86mol/L=1.14mol/L,故第Ⅱ阶段中B的平衡转化率αⅡ(B)=
| 1.14mol/L |
| 3mol/L |
C.第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡常数只受温度影响,第Ⅰ阶段与第Ⅱ阶段的温度相同,故平衡常数KⅠ=KⅡ,故C错误;
D.第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,故D正确;
故选D.
点评:本题考查化学平衡图象问题,涉及化学反应速率计算、化学平衡有关计算、化学平衡影响因素等,难度中等,注意根据瞬间浓度的变化,判断第一次平衡到第二次平衡采取的措施.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
在温度,容积相同的3个密闭容器中,按不同方式投入反应物,在保持恒温、恒容条件下发生如下反应:3X(g)+Y(g)?2Z(g)△H<0,测得相关数据如下表:
|
下列图示与对应的叙述相符的是( )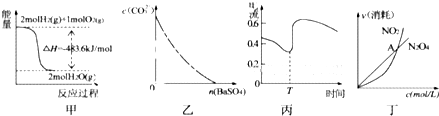

| A、图甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 | B、图乙表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化 | C、图丙表示Zn、Cu和稀硫酸构成的原电池在工作过程中电流强度的变化,T时加入了H2O2 | D、图丁表示恒温恒容条件下发生的可逆反应2NO2?N202(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
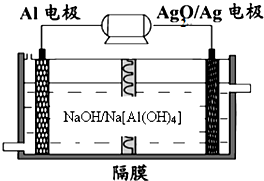 (2013?青岛一模)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
(2013?青岛一模)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用. (2012?百色二模)在2L的密闭容器内投入一定量NO2,发生反应2NO2(g)?2NO(g)+O2(g).分别在a、b两种不同实验条件下反应,得出NO2的浓度随时间变化的曲线如图所示.
(2012?百色二模)在2L的密闭容器内投入一定量NO2,发生反应2NO2(g)?2NO(g)+O2(g).分别在a、b两种不同实验条件下反应,得出NO2的浓度随时间变化的曲线如图所示.