题目内容
【题目】CuCl为白色粉末,微溶于水,溶于浓盐酸或NaCl浓溶液,不溶于乙醇。一种由海绵铜(Cu和少量CuO等)为原料制备CuCl的工艺流程如下:
(1)“溶解浸取”时,下列措施不能提高铜的浸取率的是__________(填序号)。
a.将海绵铜粉末与水搅拌成浆液 b.投料时,NaNO3适当过量
c.缩短浸取时间 d.将滤渣1返回再次溶解浸取
(2)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图-1、图-2所示:
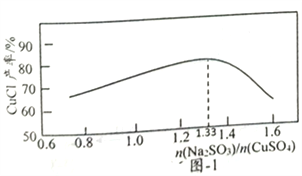

①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离了方程式为__________。
②当n(Na2SO3)/n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是__________。
③当1.0<n(NaCl)/n(CuSO4)<1.5时,比值越大CuCl产率越大,其原因是__________。
(3)“过滤2”所得滤液中溶质的主要成分为__________(填化学式)。
(4)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为__________。
【答案】 c 2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H+ 随着n(Na2SO3)/n(CuSO4)不断增大,溶液的碱性不断增强,Cu2+及CuCl的水解程度增大 适当增大c(Cl-),有利于平衡Cu+(aq)+Cl-(aq)![]() CuCl(s)向生成CuCl方向移动 Na2SO4 4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl
CuCl(s)向生成CuCl方向移动 Na2SO4 4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl
【解析】(1)a.将海绵铜粉末与水搅拌成浆液,增大反应的接触面积,能提高铜的浸取率;b.投料时,NaNO3适当过量,有利于铜的溶解,能提高铜的浸取率;c.缩短浸取时间铜可能还没完全浸取出来,降低铜的浸取率; d.将滤渣1返回再次溶解浸取,能提高铜的浸取率;答案选c;(2)①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离了方程式为2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H+;②当n(Na2SO3)/n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是随着n(Na2SO3)/n(CuSO4)不断增大,溶液的碱性不断增强,Cu2+及CuCl的水解程度增大;③当1.0<n(NaCl)/n(CuSO4)<1.5时,比值越大CuCl产率越大,其原因是适当增大c(Cl-),有利于平衡Cu+(aq)+Cl-(aq)![]() CuCl(s)向生成CuCl方向移动;(3)CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl 沉淀和Na2SO4,“过滤2”所得滤液中溶质的主要成分为Na2SO4;(4)CuCl被氧化为Cu2(OH)3Cl的化学方程式为4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl。
CuCl(s)向生成CuCl方向移动;(3)CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl 沉淀和Na2SO4,“过滤2”所得滤液中溶质的主要成分为Na2SO4;(4)CuCl被氧化为Cu2(OH)3Cl的化学方程式为4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl。

 新思维寒假作业系列答案
新思维寒假作业系列答案

