题目内容
下列分离物质的方法中,根据微粒大小进行分离的是( )
①分液 ②过滤 ③分馏 ④重结晶 ⑤渗析
A.②⑤ B.②④ C.①② D.①③⑤
根据下列实验现象,所得结论正确的是( )
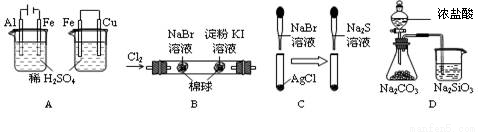
实验 | 实验现象 | 结论 |
A | 左烧杯中铁表面有气泡,右边铜表面有气泡 | 活动性:Al>Fe>Cu |
B | 左边棉花变为橙色,右边棉花变为蓝色 | 还原性:Cl-<Br-<I- |
C | 白色固体先变为淡黄色,后变为黑色 | 溶解性AgCl<AgBr<Ag2S |
D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 不能说明非金属性:Cl>C>Si |
煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。回答下列问题:
(1) NaClO2的化学名称为____________。
(2)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10?3mol·L?1。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO42? | SO32? | NO3? | NO2? | Cl? |
c/(mol·L?1) | 8.35×10?4 | 6.87×10?6 | 1.5×10?4 | 1.2×10?5 | 3.4×10?3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式 。增加压强,NO的转化率________________(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐___________(填“增大”“不变”或“减小”)。
③由实验结果可知,脱硫反应速率___________脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
(3)不同温度下,NaClO2溶液脱硫、脱硝反应中,SO2和NO的平衡分压Pe如图所示。

①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均____________(填“增大”、“不变”或“减小”)。
②反应ClO2?+2SO32?===2SO42?+Cl?的平衡常数K表达式为___________。
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是_______。
②已知下列反应:
SO2(g)+2OH? (aq)===SO32? (aq)+H2O(l) ΔH1
ClO? (aq)+SO32? (aq)===SO42? (aq)+Cl? (aq) ΔH2
CaSO4(s)===Ca2+(aq)+SO42?(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO? (aq) +2OH? (aq) === CaSO4(s) +H2O(l) +Cl? (aq)的ΔH= _。


 O2(g)=SO2(g)+H2O(g) △H1
O2(g)=SO2(g)+H2O(g) △H1 S2(g)+2H2O (g) △H2
S2(g)+2H2O (g) △H2 O2(g)=S(g)+H2O(g) △H3
O2(g)=S(g)+H2O(g) △H3 (△H1+△H2+3△H3 )
(△H1+△H2+3△H3 ) (3△H3-△H1-△H2)
(3△H3-△H1-△H2) (△H1+△H2-3△H3)
(△H1+△H2-3△H3) (△H1-△H2-3△H3)
(△H1-△H2-3△H3)