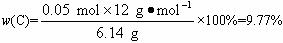题目内容
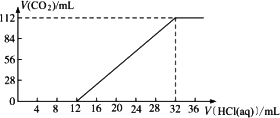
有某种碱金属元素组成的两种碳酸盐的混合物
试计算:
(1)混合物中碳元素的质量分数。
(2)确定这两种碳酸盐的化学式。
(3)所滴加盐酸的物质的量浓度。
解析:(1) n(C)=n(CO2)=![]() =0.005 mol
=0.005 mol
w(C)=![]() %=9.77%
%=9.77%
(2)混合物的平均摩尔质量![]() =
=
若M(M2CO3)=
若M(MHCO3)=
所以碱金属元素是钾元素,两种碳酸盐的化学式:K2CO3、KHCO3
(3)n(K2CO3)+n(KHCO3)=0.05 mol
n(K2CO3)×
n(K2CO3)=0.03 mol n(KHCO3)=0.02 mol
n(K2CO3)—2n(HCl) n(KHCO3)—n(HCl)
0.03 mol 0.06 mol 0.02 mol 0.02 mol
所以n(HCl)=0.06 mol+0.02 mol=0.08 mol
c(HCl)=![]() =2.5 mol·L-1
=2.5 mol·L-1
答案:(1)9.77% (2)K2CO3、KHCO3 (3)2.5 mol·L-1

练习册系列答案
相关题目