题目内容
A、B、C、D均为中学化学常见物质,且含有一种相同的 元素,它们之间有如下转化关系,其中A是单质。

(1)若A是一种淡黄色固体,B是气态氢化物,C、D为气态氧化物,且C是形成酸雨的主要物质。请写出C与B反应的化学方程式_________________________________。
(2)若B是气态氢化物,C、D为气态氧化物,且C、D是形成光化学烟雾的一个重要原因。请写出反应③的化学方程式____________________________________。实验室中检验气体B存在用的试剂或用品为________________。
(3)若B、D既能溶于强酸溶液,又能溶于强碱溶液,反应②③均需要强碱性溶液,反应④可以通过滴加少量稀盐酸实现。据此判断A元素在周期表中的位置是_________________。请写出②的离子方程式___________________________________。
(4)若C是一种淡黄色固体,常用于吸吸面具中的供氧剂,D是一种强碱。写出反应④的离子方程式___________________________________。
(1)2H2S+SO2=3S+2H2O
(2)4NH3+5O2 =4NO +6H2O ,湿润的红色石蕊试纸
(3)第三周期第ⅢA族,2Al +2OH- +6 H2O=2[Al(OH) 4] - +3H2 ↑
(4)2Na2O2+2H2O =4Na+ +4OH- +O2↑
【解析】
试题分析:(1) A是一种淡黄色固体且C是形成酸雨的主要物质,这样可以推出A为单质硫。C为SO2,而B为H2S。(2)C、D是形成光化学烟雾的一个重要原因,可以推出为氮的氧化物。由此B为NH3。检验NH3用,湿润的红色石蕊试纸。(3)B、D既能溶于强酸溶液,又能溶于强碱溶液,推出为Al元素。又因为②③均需要强碱性溶液,所以A为Al,B为Al2O3 .(4) 因为C是一种淡黄色固体,常用于吸吸面具中的供氧剂,D是一种强碱。所以C为Na2O2。
考点:考察S 、N、Al、Na的性质

 名校课堂系列答案
名校课堂系列答案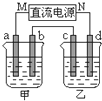 如图所示的装置中,甲、乙两烧杯中分别盛放有足量的CuSO4溶液和100g 10.00%的K2SO4溶液,a、b、c、d均为石墨电极.接通电源一段时间后,测得乙中K2SO4溶液浓度为10.47%,甲中a电极的质量增加.下列说法正确的是( )
如图所示的装置中,甲、乙两烧杯中分别盛放有足量的CuSO4溶液和100g 10.00%的K2SO4溶液,a、b、c、d均为石墨电极.接通电源一段时间后,测得乙中K2SO4溶液浓度为10.47%,甲中a电极的质量增加.下列说法正确的是( )| A、甲、乙溶液的pH均减小 | B、电极b上生成气体的体积约为2.8L(标准状况下) | C、电极d上发生的反应为:2H2O+2e-?H2↑+2OH- | D、欲使甲中的溶液恢复至原来的浓度,可加入24.5g的Cu(OH)2 |
 A、B、C、D均为常见物质,相互之间的关系如图所示.“-”表示两种物质间能发生反应,“→”表示物质间的转化关系,部分反应物或生成物以及反应条件已略去).
A、B、C、D均为常见物质,相互之间的关系如图所示.“-”表示两种物质间能发生反应,“→”表示物质间的转化关系,部分反应物或生成物以及反应条件已略去).
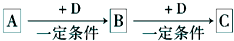 A、B、C、D均为中学化学中常见的物质,它们之间的转化关系如下图(部分产物已略去):试回答:
A、B、C、D均为中学化学中常见的物质,它们之间的转化关系如下图(部分产物已略去):试回答:
 A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素:A、B、C三种元素的原子序数之和为31;D元素与A、B、C三种元素既不是同周期,也不同主族.请回答:
A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素:A、B、C三种元素的原子序数之和为31;D元素与A、B、C三种元素既不是同周期,也不同主族.请回答:
 NH3?H2O+H+
NH3?H2O+H+ 2NH3
2NH3
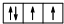 .甲和丙可形成两种化合物X和Y,X和水反应后生成一种具有还原性的二元酸M.1mol乙与足量丙可化合生成Z,所得的Z与热水反应的产物W需用12mol KOH才能完全中和.乙在足量丁中燃烧生成化合物N,N和水反应生成W和D元素的气态氢化物.试回答下列问题:
.甲和丙可形成两种化合物X和Y,X和水反应后生成一种具有还原性的二元酸M.1mol乙与足量丙可化合生成Z,所得的Z与热水反应的产物W需用12mol KOH才能完全中和.乙在足量丁中燃烧生成化合物N,N和水反应生成W和D元素的气态氢化物.试回答下列问题: