题目内容
(10分) 有人设计了如下甲醇(methanol) 合成工艺:

其中,①为甲烷气源,压强250.0kPa,温度25oC,流速55.0 m3s-1。②为水蒸气源,压强200.0kPa,温度150oC,流速150.0 m3s-1。合成气和剩余反应物的混合物经管路③进入25oC的冷凝器(condenser),冷凝物由管路⑤流出。在B中合成的甲醇和剩余反应物的混合物经⑥进入25oC的冷凝器,甲醇冷凝后经管路⑦流出,其密度为0.791gmL-1。
12-1. 分别写出在步骤A和步骤B中所发生的化学反应的方程式。
12-2. 假定:所有气体皆为理想气体,在步骤A和B中完全转化,气液在冷凝器中完全分离,计算经步骤A和步骤B后,在一秒钟内剩余物的量。
12-3. 实际上,在步骤B中CO的转化率只有三分之二。计算在管路⑥中CO、H2和CH3OH的分压(总压强为10.0 MPa)。
12-4. 当甲醇反应器足够大,反应达到平衡,管路⑥中的各气体的分压服从方程
12-1. CH4(g)+H2O(g)=CO(g)+3H2(g) (1分)
CO(g)+2H2(g)=CH3OH(g) (1分)
12-2. n(CH4)=(250.0×103×55.0)/(8.314×298) =5.55×103(mol)
n [H2O(g)]=(200.0×103×150.0)/(8.314×423) =8.53×103(mol)经步骤A后在③中过量的H2O(g)=(8.53×103-5.55×103) mol =2.98×103 mol (1 分)
在步骤A中生成的CO和H2的摩尔比为1:3,而在步骤B中消耗的CO和H2的摩尔比为1:2,故经步骤B后剩余的H2为5.55×103mol (1)
12-3. nT = n(CO)+n(H2)+n(CH3OH)
={5.55×103×1/3+(16.65×103-5.55×103×2/3×2) +5.55×103×2/3}mol
= 14.8×103mol (1 分)
p(i)= pT×ni/nT总
p(CO) =10.0 MPa×(5.55×103×1/3/14.8×103) = 0.125 MPa (1分)
p(H2) =10.0 MPa×(9.25×103/14.8×103) =0.625 MPa ( 1分)
p(CH3OH) =10.0 MPa×(5.55×103×2/3/14.8×103) = 0.250 MPa ( 1分)
12-4. ![]()
式中p0=0.100 MPa, 计算平衡常数Kp。
Kp=0.250×(0.100)2/(0.125×0.6252) = 5.12×10-2

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案(10 分)SO2和NOx的排放是造成酸雨的两大罪魁祸首。下图表示了某地区在1940~2002年间,空气中SO2和NOx含量因燃料燃烧、工业生产、交通运输以及其他因素的影响而发生变化的基本统计数据。

(1)结合上图数据,判断下列说法正确的是 ▲ 。
A.在交通运输中排放的NOx与燃料的不充分燃烧有关
B.在上世纪60年代以前,在交通运输中排放的SO2主要是使用燃煤的内燃机所致
C.近年来在工业生产中SO2排放量的下降,主要是减少了燃烧的煤的质量
D.随着汽车工业的发展,在形成酸雨的因素中,NOx所占比重在逐渐增大
(2)在上图表示的历史进程中,由工业生产所导致的SO2的排放量明显地在逐年减少。请用化学方程式说明人类在为解决SO2污染问题中所进行的一个反应过程:
▲ 。
(3)汽车排放的尾气中含有未燃烧充分的CmHn、以及N2、CO2、NO、CO等。有人设计利用反应2NO + 2CO  N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
|
时间/h |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)/mol·L-1 |
1.00×10-3 |
4.5×10-4 |
2.5×10-4 |
1.5×10-4 |
1.00×10-4 |
1.00×10-4 |
|
c(CO)/mol·L-1 |
3.6×10-3 |
3.05×10-3 |
2.85×10-3 |
2.75×10-3 |
2.70×10-3 |
2.70×10-3 |

 在上述条件下反应能够自发进行,则反应的
在上述条件下反应能够自发进行,则反应的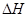 ▲ 0(“>”、“<”、“=”)。
▲ 0(“>”、“<”、“=”)。 在该温度下,反应的平衡常数K= ▲ 。
在该温度下,反应的平衡常数K= ▲ 。
(4)某次降雨过程收集到10L的雨水,向雨水中滴加1mL6mol/L的H2O2,充分反应后测得溶液的pH=3.62 [c(H+) =2.4×10-4 mol/L ]),再向溶液中加入足量的Ba(OH)2溶液,经过滤、晾干、称重,得沉淀的质量为0.1864g。若假设雨水的酸性仅由NOx和SO2的排放所致。请计算排放在空气中的NOx和SO2的物质的量之比接近于 ▲ 。



 Sx 、
Sx 、 Sx 。其中COS中“C”化合价为 。
Sx 。其中COS中“C”化合价为 。