题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、常温常压下,11.2L Cl2含有的分子数为0.5NA |
| B、常温常压下,1mol 氦气含有的原子数为NA |
| C、NA 个CO2分子占有的体积不一定为22.4L |
| D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据气体摩尔体积条件应用分析,标准状况气体摩尔体积为224L/mol;
B、氦气是单原子分子;
C、NA 个CO2分子物质的量为1mol,标准状况气体体积为22.4L;
D、溶液体积不知不能计算微粒数.
B、氦气是单原子分子;
C、NA 个CO2分子物质的量为1mol,标准状况气体体积为22.4L;
D、溶液体积不知不能计算微粒数.
解答:
解:A、依据气体摩尔体积条件应用分析,标准状况气体摩尔体积为224L/mol,常温常压下,11.2L Cl2含物质的量不是0.5mol,故A错误;
B、氦气是单原子分子,1mol 氦气含有的原子数为NA,故B正确;
C、NA 个CO2分子物质的量为1mol,标准状况气体体积为22.4L,温度压强不知,NA 个CO2分子占有的体积不一定为22.4L,故C正确;
D、溶液体积不知不能计算微粒数,故D错误;
故选BC.
B、氦气是单原子分子,1mol 氦气含有的原子数为NA,故B正确;
C、NA 个CO2分子物质的量为1mol,标准状况气体体积为22.4L,温度压强不知,NA 个CO2分子占有的体积不一定为22.4L,故C正确;
D、溶液体积不知不能计算微粒数,故D错误;
故选BC.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件分析应用,注意物质结构分析判断,掌握基础是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各项是关于玻璃棒在若干实验中的用途及操作,其中错误的是( )
①溶解物质时搅拌
②蒸发操作时搅拌液体防止暴沸
③蘸取少量溶液测其pH
④过滤时用玻璃棒引流,其下端在漏斗内滤纸的任意部位
⑤配制一定体积的物质的量浓度的溶液用玻璃棒引流
⑥加热坩埚中固体物质用玻璃棒翻炒固体.
①溶解物质时搅拌
②蒸发操作时搅拌液体防止暴沸
③蘸取少量溶液测其pH
④过滤时用玻璃棒引流,其下端在漏斗内滤纸的任意部位
⑤配制一定体积的物质的量浓度的溶液用玻璃棒引流
⑥加热坩埚中固体物质用玻璃棒翻炒固体.
| A、①③⑤ | B、③④⑥ |
| C、只有④ | D、全部错误 |
下表是某同学血常规检验报告单中的部分内容,该同学应注意补充的微量元素是( )
| 编号 | 项目 | 结果 | 正常范围参考值 | 单位 |
| 1 | 红细胞计数 | 2.1 | 3.5~5 | ×1012?L-1 |
| 2 | 血红蛋白 | 73 | 110~150 | g?L-1 |
| A、硒 | B、锌 | C、铁 | D、碘 |
下列应用特征现象推断不正确的是( )
| A、遇FeCl3溶液显紫色或加入溴水产生白色沉淀,表示物质中可能含有酚羟基 |
| B、加入新制Cu(OH)2悬浊液并加热,有红色沉淀生成,或加入银氨溶液并水浴加热有银镜出现,说明该物质中含有-CHO |
| C、加入金属钠,有H2产生,表示物质可能有-OH或-COOH |
| D、加入NaHCO3溶液有气体放出或能使紫色石蕊试液变红,表示物质中含有-COOH |
 某化工生产反应历程的能量变化如图,过程I没有使用催化剂,过程Ⅱ使用了催化剂,则可判断催化剂除了能改变反应速率外,还可以改变的是( )
某化工生产反应历程的能量变化如图,过程I没有使用催化剂,过程Ⅱ使用了催化剂,则可判断催化剂除了能改变反应速率外,还可以改变的是( )| A、反应物的熔沸点 |
| B、反应的完成程度 |
| C、生产能耗 |
| D、反应热效应 |
 )具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )
)具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是( )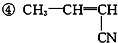 ⑤CH3-CH═CH2.
⑤CH3-CH═CH2. (1)标准状况下,CO2分子数为6.02×1023,CO2的物质的量为
(1)标准状况下,CO2分子数为6.02×1023,CO2的物质的量为