题目内容
常温下向20 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液40 mL,溶液pH逐渐降低,此时溶液中含碳元素的微粒的物质的量浓度的百分含量(纵轴)发生的变化(CO2因逸出未画出)如图所示,根据图示回答下列问题:

(1)20 mL 0.1 mol·L-1 Na2CO3溶液呈碱性的原因是(用离子方程式表示)________.
(2)当反应到A点时,溶液中所有阳离子和阴离子的浓度大小关系为________.
(3)B点表示的含义是________.
(4)当混合液的pH=________时,开始放出CO2气体.
答案:
解析:
解析:
|
(1)CO (2)c(Na+)>c(CO (3)Na2CO3恰好转化为NaHCO3,此时溶液的pH为8 (4)6 |

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
|
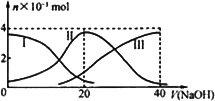
常温下,向20 mL 0.2 mol·L-1 H2A溶液中滴加0.2 mol·L-1 NaOH溶液.有关微粒的物质的量(n)变化如下图.(其中Ⅰ表示H2A,Ⅱ代表HA-、Ⅲ代表A2-.)根据图示判断,当V(NaOH)=20 mL时,溶液中各粒子浓度的大小顺序正确的是
| |
| [ ] | |
A. |
c(Na+)>c(HA-)>c(OH-)>c(H2A)>c(H+)>c(A2-) |
B. |
c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)>c(H2A) |
C. |
c(Na+)>c(H+)>c(HA-)>c(A2-)>c(OH-)>c(H2A) |
D. |
c(Na+)>c(OH-)>c(HA-)>c(H2A)>c(H+)>c(A2-) |