题目内容
| |||||||||||||||||||||||||||||||||||||
答案:1.ABE;
解析:
解析:
(2) |
除去Fe3+ |
(3) |
是 |
(4) |
< |
(5) |
CaCl2+H2O2 加入NaOH溶液使上述平衡向正反应方向,有利于CaO2沉淀的生成. |
(6) |
25n/18am |

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目



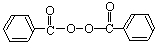 )和过氧化钙(CaO2)。下列关于“面粉增白剂”的说法不正确的是(
)
)和过氧化钙(CaO2)。下列关于“面粉增白剂”的说法不正确的是(
)