题目内容
11.有机化合物A的相对分子质量为134,A仅含碳、氢、氧三种元素,且分子中含有甲基.A既可以与乙醇发生酯化反应,又可以与乙酸发生酯化反应,且测得A与乙醇完全酯化所得有机产物的相对分子质量为190.据此写出A的分子式C4H6O5,结构简式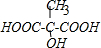 .
.
分析 A仅含碳、氢、氧三种元素,既可以与乙醇发生酯化反应,又可以与乙酸发生酯化反应,则A分子中含有羧基、羟基,测得A与乙醇完全酯化所得有机物B的相对分子质量为190,A的相对分子质量为134,设A分子中羧基数目为x,则134+46x=190+18x,解得x=2;A分子中至少含有2个-COOH、1个-OH、1个甲基,去掉22个-COOH、1个-OH、1个甲基剩余总相对原子质量质量为:134-45×2-17-15×1=12,则应该还含有1个亚甲基(-CH2-),据此确定其分子式、结构简式.
解答 解:A仅含碳、氢、氧三种元素,既可以与乙醇发生酯化反应,又可以与乙酸发生酯化反应,则A分子中含有羧基、羟基,
测得A与乙醇完全酯化所得有机物B的相对分子质量为190,A的相对分子质量为134,设A分子中羧基数目为x,则134+46x=190+18x,解得x=2;
A分子中至少含有2个-COOH、1个-OH、1个甲基,去掉22个-COOH、1个-OH、1个甲基剩余总相对原子质量质量为:134-45×2-17-15×1=12,则应该还含有1个亚甲基(-CH2-),
所以A的结构简式为: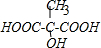 ,分子式为:C4H6O5,
,分子式为:C4H6O5,
故答案为:C4H6O5;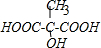 .
.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,熟练掌握常见有机物结构与性质为解答关键,试题充分考查了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
2.X~R是元素周期表中的短周期元素,其相应信息如表:
请用化元素学用语回答下列问题:
(1)X在周期表中的位置是第三周期ⅦA族
(2)元素W的离子结构示意图为
(3)元素R的最高价氧化物的电子式为
(4)X的氢化物和Z的氢化物反应形成化合物A,A中含有的化学键类型有离子键、共价键;将A溶于水,其水溶液中离子浓度由大到小的顺序是c(Cl-)>c(NH4+)>c(H+)>c(OH-)
(5)含Y的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是(用离子方程式表示)Al3++3H2O=Al(OH)3(胶体)+3H+
(6)W2O2常用作舰艇、航天器的供氧剂,写出体现其反应原理的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
| 元素 | X | Y | Z | W | R |
| 相 关 信 息 | 能形成+7价的化合物 | 日常生活中常见的金属,熔化时并不滴落,好像有一层膜兜着 | 通常状况下能形成短周期中最稳定的双原子分子,它是空气的主要成分之一 | 焰色反应为黄色 | 位于第ⅣA族,是形成化合物种类最多的元素 |
(1)X在周期表中的位置是第三周期ⅦA族
(2)元素W的离子结构示意图为

(3)元素R的最高价氧化物的电子式为

(4)X的氢化物和Z的氢化物反应形成化合物A,A中含有的化学键类型有离子键、共价键;将A溶于水,其水溶液中离子浓度由大到小的顺序是c(Cl-)>c(NH4+)>c(H+)>c(OH-)
(5)含Y的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是(用离子方程式表示)Al3++3H2O=Al(OH)3(胶体)+3H+
(6)W2O2常用作舰艇、航天器的供氧剂,写出体现其反应原理的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
16.已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4.则下列说法不正确的是( )
| A. | 气态氢化物的稳定性:HX>H2Y>ZH3 | B. | 非金属活泼性:Y<X<Z | ||
| C. | 单质的氧化性:X>Y>Z | D. | 原子最外电子层上电子数不等 |
3.如图是一原电池的装置,关于它的说法正确的是( )


| A. | 装置中铜是负极 | |
| B. | 铜表面的反应为:2H++2e-=H2↑ | |
| C. | 电流的方向是从铁经导线流向铜 | |
| D. | 构成原电池后,铁与硫酸铜的反应速率加快 |
20.环氧树脂具有极强的粘结性,俗称“万能胶”.双酚A是制备环氧树脂的重要原料,其结构为 .下列有关双酚A的叙述不正确的是( )
.下列有关双酚A的叙述不正确的是( )
 .下列有关双酚A的叙述不正确的是( )
.下列有关双酚A的叙述不正确的是( )| A. | 能和NaOH溶液反应 | B. | 能和FeCl3溶液发生显色反应 | ||
| C. | 能和浓溴水反应 | D. | 苯环上一溴代物有四种 |
1.下列关于元素周期表和元素周期律的说法不正确的是( )
| A. | 从氟到碘,其氢化物的稳定性逐渐减弱 | |
| B. | 因为铝原子比钠原子失去电子数目多,所以铝比钠的还原性强 | |
| C. | 第三周期从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强 | |
| D. | 氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强 |





