题目内容
与c(H+)·c(OH-)=KW类似,FeS饱和溶液中存在:FeS(s)(1)理论上FeS的溶解度为___________________。
(2)又知FeS饱和溶液中c(H+)与c(S2-)之间存在以下限量关系:c2(H+)·c(S2-)=1.0×10-22,为了使溶液里c(Fe2+)达到1 mol·L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)为_________________。
解析:(1)由FeS(s) ![]() Fe2++S2-得
Fe2++S2-得
c(Fe2+)=![]() =9×10-9 mol·L-1
=9×10-9 mol·L-1
即1 L水中可溶解9×10-9 mol的 FeS。
由100∶S=1 000∶(9×10-9×88) g
所以S=7.92×10-8 g。
(2)c(Fe2+)=1 mol·L-1,则
c(S2-)=![]() =8.1×10-17 mol·L-1。
=8.1×10-17 mol·L-1。
又c2(H+)·c(S2-)=1.0×10-22,所以
c(H+)= =1.11×10-3 mol·L-1。
=1.11×10-3 mol·L-1。
答案:(1)7.92×10-8 g
(2)1.11×10-3 mol·L-1

 阅读快车系列答案
阅读快车系列答案有机物在反应中常有原子问的共价键全部或部分断裂,如C-H、C-C、C=C、C-0、C=O等.下列各反应中,反应物分子中断裂键的正确组合是( )
|
[化学—选修3:物质结构与性质](15分)
硅是重要的半导体材料,构成了现代电子工业的基础。请回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 、电子数为 。
(2)硅主要以硅酸盐、 等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以 相结合,其晶胞中共有8个原子,其中在面心位置贡献 个原子。
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为 。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
|
化学键 |
C—C |
C—H |
C—O |
Si—Si |
Si—H |
Si—O |
|
键能/(kJ?mol-1 |
356 |
413 |
336 |
226 |
318 |
452 |
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是 。
②SiH4的稳定性小于CH4,更易生成氧化物,原因是 。
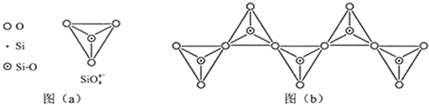
(6)在硅酸盐中,SiO4- 4四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为 ,Si与O的原子数之比为 ,化学式为 。

 W是某短周期元素X的固态单质,A、B、C均为含X元素的酸式钠盐,它们在一定条件下有如图所示的转化关系,其中某些反应产物中的
W是某短周期元素X的固态单质,A、B、C均为含X元素的酸式钠盐,它们在一定条件下有如图所示的转化关系,其中某些反应产物中的