��Ŀ����
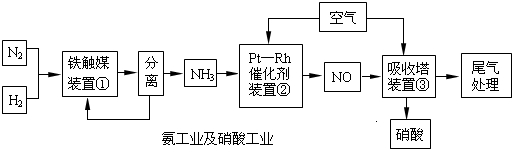
��ҵ�ϳɰ����Ʊ�����һ��������������������£�
��1����ҵ����ʱ����ȡ������һ����ӦΪ��CO+H2O��g��?CO2+H2
��t��ʱ����1L�ܱ������г���0.2mol CO��0.3molˮ��������Ӧ����ƽ�����ϵ��c��H2��=0.12mol?L-1�����¶��´˷�Ӧ��ƽ�ⳣ��K=______ �������������
�ڱ����¶Ȳ��䣬������ƽ����ϵ���ټ���0.1molCO������Ӧ���½���ƽ��ʱ��ˮ������ת���ʦ���H2O��=______��
�� ��2���ϳ����з�����ӦN2��g��+3H2��g��?2NH3��g������H��0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������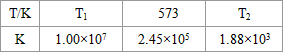
T1______573K�����������������=������
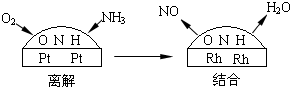
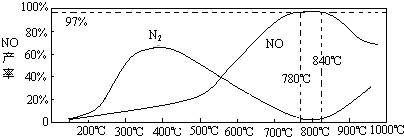
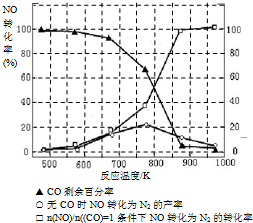
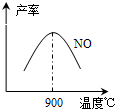 ��3��NH3��O2�ڲ�ϵ���������´�145��Ϳ�ʼ��Ӧ��4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H=-905kJ?mol-1����ͬ�¶���NO��������ͼ��ʾ���¶ȸ���900��ʱ��NO�����½���ԭ��______��
��3��NH3��O2�ڲ�ϵ���������´�145��Ϳ�ʼ��Ӧ��4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H=-905kJ?mol-1����ͬ�¶���NO��������ͼ��ʾ���¶ȸ���900��ʱ��NO�����½���ԭ��______��
��4����ˮ�е�N��PԪ�������ˮ�帻Ӫ�����Ĺؼ����أ�ũҩ���ŷŵķ�ˮ�г����н϶��NH4+��PO43-��һ�����ͨ�����ַ��������ȥ��
�ٷ���һ����Ca��OH��2��CaO Ͷ�ӵ��������ķ�ˮ�У���������ƣ��Ӷ����л��գ���������ķ�ˮ��c��Ca2+��=2��10-7 mol/Lʱ����Һ��c��PO43-��=______mol/L��
����֪Ksp[Ca3��PO4��2]=2��10-33��
�ڷ��������ڷ�ˮ�м���þ��ҵ��ˮ���Ϳ������ɸ�Ʒλ����ʯ-���ʯ����Ӧ�ķ���ʽΪMg2++NH4++PO43-=MgNH4PO4�����÷�������Ҫ������ˮ��pHΪ7.5��10����pH����10.7�����ʯ�IJ������ͣ���ԭ�����Ϊ______���뷽��һ��ȣ����������ŵ�Ϊ______��
�⣺��1���ٸ������⣺CO+H2O��g��?CO2 +H2
��ʼŨ�ȣ�0.2 0.3 0 0
�仯Ũ�ȣ�0.12 0.12 0.12 0.12
ƽ��ʱ��Ũ�ȣ�0.08 0.18 0.12 0.12 ��K=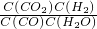 =
=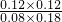 =1��
=1��
�ʴ�Ϊ��1��
�ڱ����¶Ȳ��䣬������ƽ����ϵ���ټ���0.1molCO���൱�ڳ���0.3molCO��0.3molˮ��������H2O��ת����xmol
CO+H2O��g��?CO2 +H2
��ʼ��0.3 0.3 0 0
ת����x x x x
ƽ��0.3-x 0.3-x x x ��K=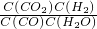 =
=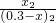 =1��x=0.15��ˮ��������ת���ʦ���H2O��=
=1��x=0.15��ˮ��������ת���ʦ���H2O��=
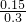 ��100%=50%��
��100%=50%��
�ʴ�Ϊ��50%��
��2�����ڷ��ȷ�Ӧ���¶�Խ�ߣ���ѧƽ�������ƶ����ϳ����з�����ӦN2��g��+3H2��g��?2NH3��g������H��0������ӦΪ���ȷ�Ӧ����ѧƽ�������ƶ�������ƽ�ⳣ����С������T1��573K��
�ʴ�Ϊ����
��3�����ڷ��ȷ�Ӧ���¶����ߣ���ѧƽ���������ƶ�����ӦN2��g��+3H2��g��?2NH3��g������H��0������ӦΪ���ȷ�Ӧ���������IJ��ʼ�С��
�ʴ�Ϊ���¶ȸ���900��ʱ��ƽ�������ƶ���
��4���ٷ�ˮ��c��Ca2+��=2��10-7 mol/Lʱ������Ksp[Ca3��PO4��2]=c3��Ca2+����c2��PO43-��=8.0��10-21��c2��PO43-��=2.0��10-33�����c��PO43-��=5.0��10-7mol?L-1��
�ʴ�Ϊ��5��10-7��
����pH����10.7�����ʯ�IJ������ͣ���������Һ�е�Mg2+��NH4+����OH-��Ӧ��ƽ�����淴Ӧ�����ƶ�����������ͬʱ��ȥ��ˮ�еĵ������������þ��ҵ��ˮ��
�ʴ�Ϊ����pH����10.7ʱ����Һ�е�Mg2+��NH4+����OH-��Ӧ��ƽ�����淴Ӧ�����ƶ�����ͬʱ��ȥ��ˮ�еĵ������������þ��ҵ��ˮ��
��������1���ٸ���ƽ�ⳣ������ʽ�Լ��������ʵ�Ũ��֪ʶ���ش�
�ڸ���CO+H2O��g��?CO2+H2���������ʵ�Ũ�Ƚ��м��㣻
��2�������¶Ⱥ�ƽ�ⳣ����Ĺ�ϵ�Լ�ƽ�ⳣ�����¶ȵ�Ӱ��������
��3�����ڷ��ȷ�Ӧ���¶����ߣ���ѧƽ���������ƶ���
��4���ٸ���Ksp[Ca3��PO4��2]=2.0��10-33���㣻
����pH����10.7�����ʯ�IJ������ͣ���������Һ�е�Mg2+��NH4+����OH-��Ӧ����������ͬʱ��ȥ��ˮ�еĵ���
������������Ҫ�����˹�ҵ�ϳɰ����Ʊ����ᣬ�ص㿼����ƽ�ⳣ���ļ��㣬�ۺ���ǿ���ѶȽϴ��Ը�����ѧ֪ʶ���лش�ƽʱע�����������������
��ʼŨ�ȣ�0.2 0.3 0 0
�仯Ũ�ȣ�0.12 0.12 0.12 0.12
ƽ��ʱ��Ũ�ȣ�0.08 0.18 0.12 0.12 ��K=
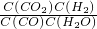 =
=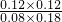 =1��
=1���ʴ�Ϊ��1��
�ڱ����¶Ȳ��䣬������ƽ����ϵ���ټ���0.1molCO���൱�ڳ���0.3molCO��0.3molˮ��������H2O��ת����xmol
CO+H2O��g��?CO2 +H2
��ʼ��0.3 0.3 0 0
ת����x x x x
ƽ��0.3-x 0.3-x x x ��K=
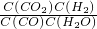 =
=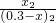 =1��x=0.15��ˮ��������ת���ʦ���H2O��=
=1��x=0.15��ˮ��������ת���ʦ���H2O��=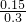 ��100%=50%��
��100%=50%���ʴ�Ϊ��50%��
��2�����ڷ��ȷ�Ӧ���¶�Խ�ߣ���ѧƽ�������ƶ����ϳ����з�����ӦN2��g��+3H2��g��?2NH3��g������H��0������ӦΪ���ȷ�Ӧ����ѧƽ�������ƶ�������ƽ�ⳣ����С������T1��573K��
�ʴ�Ϊ����
��3�����ڷ��ȷ�Ӧ���¶����ߣ���ѧƽ���������ƶ�����ӦN2��g��+3H2��g��?2NH3��g������H��0������ӦΪ���ȷ�Ӧ���������IJ��ʼ�С��
�ʴ�Ϊ���¶ȸ���900��ʱ��ƽ�������ƶ���
��4���ٷ�ˮ��c��Ca2+��=2��10-7 mol/Lʱ������Ksp[Ca3��PO4��2]=c3��Ca2+����c2��PO43-��=8.0��10-21��c2��PO43-��=2.0��10-33�����c��PO43-��=5.0��10-7mol?L-1��
�ʴ�Ϊ��5��10-7��
����pH����10.7�����ʯ�IJ������ͣ���������Һ�е�Mg2+��NH4+����OH-��Ӧ��ƽ�����淴Ӧ�����ƶ�����������ͬʱ��ȥ��ˮ�еĵ������������þ��ҵ��ˮ��
�ʴ�Ϊ����pH����10.7ʱ����Һ�е�Mg2+��NH4+����OH-��Ӧ��ƽ�����淴Ӧ�����ƶ�����ͬʱ��ȥ��ˮ�еĵ������������þ��ҵ��ˮ��
��������1���ٸ���ƽ�ⳣ������ʽ�Լ��������ʵ�Ũ��֪ʶ���ش�
�ڸ���CO+H2O��g��?CO2+H2���������ʵ�Ũ�Ƚ��м��㣻
��2�������¶Ⱥ�ƽ�ⳣ����Ĺ�ϵ�Լ�ƽ�ⳣ�����¶ȵ�Ӱ��������
��3�����ڷ��ȷ�Ӧ���¶����ߣ���ѧƽ���������ƶ���
��4���ٸ���Ksp[Ca3��PO4��2]=2.0��10-33���㣻
����pH����10.7�����ʯ�IJ������ͣ���������Һ�е�Mg2+��NH4+����OH-��Ӧ����������ͬʱ��ȥ��ˮ�еĵ���
������������Ҫ�����˹�ҵ�ϳɰ����Ʊ����ᣬ�ص㿼����ƽ�ⳣ���ļ��㣬�ۺ���ǿ���ѶȽϴ��Ը�����ѧ֪ʶ���лش�ƽʱע�����������������

��ϰ��ϵ�д�
�����Ŀ
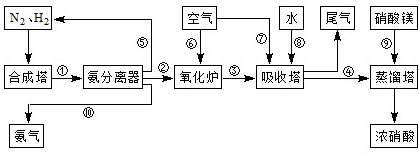
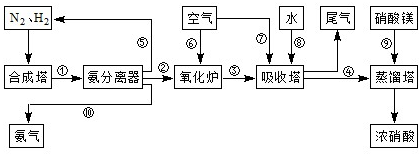
��ҵ�ϳɰ����Ʊ�����һ�������������������ͼ��
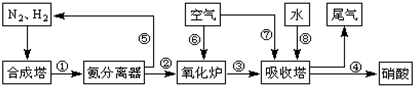
��1����ҵ����ʱ����ȡ������һ����ӦΪ��CO��g��+H2O��g��?CO2��g��+H2��g����t��ʱ����10L�ܱ������г���2mol CO��3molˮ��������Ӧ����ƽ�����ϵ��c��H2��=0.12mol?L-1������¶��´˷�Ӧ��ƽ�ⳣ��K= �������������
��2���ϳ����з�����ӦN2��g��+3H2��g��?2NH3��g����H��0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1 300�棨���������������=������
��3�������ڴ�����ȼ������һ�ֵ��ʺ�ˮ����ѧ�����ô�ԭ������Ƴɡ�����-������ȼ�ϵ�أ���ͨ�백���ĵ缫�� ����������������������������£��õ缫������Ӧ�ĵ缫��ӦʽΪ ��
��4���ð������������������ᣬ��β���е�NOx����Ⱦ������Ŀǰ��ѧ��̽������ȼ�������еļ���Ƚ����������ﻹԭΪ������ˮ����Ӧ����Ϊ��
CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ?mol-1
CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1160kJ?mol-1
�����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ ��
��5��ij�о�С����ʵ�����ԡ�Ag-ZSM-5��Ϊ��������ý�NOת��ΪN2��ת�������¶ȱ仯�������ͼ����ͼ����������ʹ��CO���¶ȳ���775�棬����NO��ת���ʽ��ͣ�����ܵ�ԭ��Ϊ ����
=1�������£�Ӧ���Ƶ�����¶��� ���ң�

��1����ҵ����ʱ����ȡ������һ����ӦΪ��CO��g��+H2O��g��?CO2��g��+H2��g����t��ʱ����10L�ܱ������г���2mol CO��3molˮ��������Ӧ����ƽ�����ϵ��c��H2��=0.12mol?L-1������¶��´˷�Ӧ��ƽ�ⳣ��K=
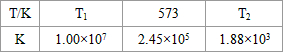
��2���ϳ����з�����ӦN2��g��+3H2��g��?2NH3��g����H��0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1
| T/�� | T1 | 300 | T2 |
| K | 1.00��107 | 2.45��105 | 1.88��103 |
��4���ð������������������ᣬ��β���е�NOx����Ⱦ������Ŀǰ��ѧ��̽������ȼ�������еļ���Ƚ����������ﻹԭΪ������ˮ����Ӧ����Ϊ��
CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ?mol-1
CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1160kJ?mol-1
�����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ
��5��ij�о�С����ʵ�����ԡ�Ag-ZSM-5��Ϊ��������ý�NOת��ΪN2��ת�������¶ȱ仯�������ͼ����ͼ����������ʹ��CO���¶ȳ���775�棬����NO��ת���ʽ��ͣ�����ܵ�ԭ��Ϊ
| n(NO) |
| n(CO) |

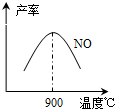 ��3��NH3��O2�ڲ�ϵ���������´�145��Ϳ�ʼ��Ӧ��4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H=-905kJ?mol-1����ͬ�¶���NO��������ͼ��ʾ���¶ȸ���900��ʱ��NO�����½���ԭ��
��3��NH3��O2�ڲ�ϵ���������´�145��Ϳ�ʼ��Ӧ��4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H=-905kJ?mol-1����ͬ�¶���NO��������ͼ��ʾ���¶ȸ���900��ʱ��NO�����½���ԭ��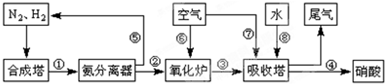
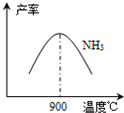 ��3��N2��H2���������������´�145��Ϳ�ʼ��Ӧ����ͬ�¶���NH3������ͼ��ʾ���¶ȸ���900��ʱ��NH3�����½���ԭ��
��3��N2��H2���������������´�145��Ϳ�ʼ��Ӧ����ͬ�¶���NH3������ͼ��ʾ���¶ȸ���900��ʱ��NH3�����½���ԭ��