��Ŀ����
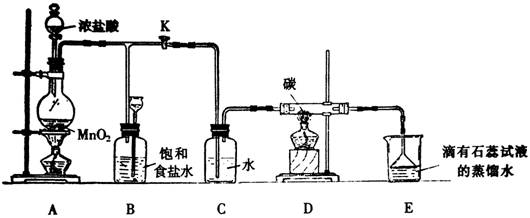
��ͼ��һ����ȡ������������Ϊԭ�Ͻ����ض���Ӧ��װ�ã�

(1)A����������װ�ã����з�����Ӧ�Ļ�ѧ����ʽΪ________��
(2)ʵ�鿪ʼʱ���ȵ�ȼA���ľƾ��ƣ�������K����Cl2��������װ�ã��ٵ�ȼD���ƾ��ƣ�������Eװ�ã�Cl2ͨ��Cƿ���ٽ���D��Dװ�õ�Ӳ�ʲ�������ʢ��̿�ۣ�����������ԭ��Ӧ�������ΪCO2��HCl����д��D�з�Ӧ�Ļ�ѧ����ʽ��________��װ��C��������________��
(3)��E������ɫʯ�����ɫ����ɫ��Ϊ��ɫ���ٱ�Ϊ��ɫ����ԭ����________��
(4)����E���ձ�����Һ��Ϊ����ʯ��ˮ����Ӧ����������Ϊ________(ѡ�����)��
A���а�ɫ��������
B�������Ե�����
C�������ɰ�ɫ�����������ɫ������ʧ
(5)D����Ӧ��Ϻر�����K����ȥ�ƾ��ƣ����������ȵ����ã�A������Cl2��������ʱB�е�������________��B��������________��
������
|
����(1)MnO2��4HCl(Ũ) ����(2)2Cl2��C��2H2O ����(3)HCl����ˮʹʯ����ɫ��������������ˮ����HClO��ʹʯ����ɫ�� ����(4)B ����(5)��Һ����©����,�������� |