题目内容
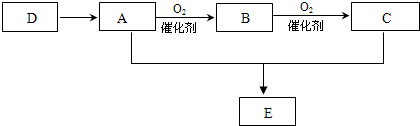
已知:A、B、C、D、E的相互转化关系如下图所示,其中D是石油裂解气的主要成分,D的产量通常用来衡量一个国家的石油化工水平,E的分子式是C4H8O2,它具有一种特殊的香味.
回答下列问题:
(1)A的结构简式是
(2)写出A+C→E的化学反应方程式
(3)有机物D可以形成具有一定用途的有机高分子材料,写出由D反应生成该有机高分子材料的化学反应方程式

回答下列问题:
(1)A的结构简式是
CH2=CH2
CH2=CH2
,有机物B所含有的官能团的名称为醛基
醛基
;(2)写出A+C→E的化学反应方程式
CH3COOH+HOC2H5
CH3COOC2H5+H2O
| 浓硫酸 |
| △ |
CH3COOH+HOC2H5
CH3COOC2H5+H2O
,该反应的类型是| 浓硫酸 |
| △ |
酯化反应
酯化反应
.(3)有机物D可以形成具有一定用途的有机高分子材料,写出由D反应生成该有机高分子材料的化学反应方程式
nCH2=CH2

| 一定条件 |

nCH2=CH2

.| 一定条件 |

分析:D是石油裂解气的主要成分,D的产量通常用来衡量一个国家的石油化工水平,则D为CH2=CH2,E的分子式是C4H8O2,它具有一种特殊的香味,E属于酯,故乙烯和水发生加成反应生成A,则A是乙醇,乙醇和氧气反应生成B,则B是乙醛,B和氧气反应生成C,C是乙酸,乙醇和乙酸反应生成乙酸乙酯,故E为CH3COOCH2CH3,
(3)中以乙烯为主要原料合成高分子化合物是聚乙烯,据此解答.
(3)中以乙烯为主要原料合成高分子化合物是聚乙烯,据此解答.
解答:解:D是石油裂解气的主要成分,D的产量通常用来衡量一个国家的石油化工水平,则D为CH2=CH2,E的分子式是C4H8O2,它具有一种特殊的香味,E属于酯,故乙烯和水发生加成反应生成A,则A是乙醇,乙醇和氧气反应生成B,则B是乙醛,B和氧气反应生成C,C是乙酸,乙醇和乙酸反应生成乙酸乙酯,故E为CH3COOCH2CH3,
(1)由上述分析可知,D为CH2=CH2,B是乙醛,含有醛基,
故答案为:CH2=CH2;醛基;
(2)A+C→E是乙酸和乙醇在浓硫酸作用下加热发生酯化或取代反应生成乙酸乙酯,反应的方程式为:CH3COOH+HOC2H5
CH3COOC2H5+H2O,
故答案为:CH3COOH+HOC2H5
CH3COOC2H5+H2O;酯化反应;
(3)以乙烯为主要原料合成高分子化合物是聚乙烯E是聚乙烯,结构简式为 ,反应方程式为:nCH2=CH2
,反应方程式为:nCH2=CH2
 ,
,
故答案为:nCH2=CH2
 .
.
(1)由上述分析可知,D为CH2=CH2,B是乙醛,含有醛基,
故答案为:CH2=CH2;醛基;
(2)A+C→E是乙酸和乙醇在浓硫酸作用下加热发生酯化或取代反应生成乙酸乙酯,反应的方程式为:CH3COOH+HOC2H5
| 浓硫酸 |
| △ |
故答案为:CH3COOH+HOC2H5
| 浓硫酸 |
| △ |
(3)以乙烯为主要原料合成高分子化合物是聚乙烯E是聚乙烯,结构简式为
 ,反应方程式为:nCH2=CH2
,反应方程式为:nCH2=CH2| 一定条件 |
 ,
,故答案为:nCH2=CH2
| 一定条件 |
 .
.点评:本题考查有机物的推断,题目难度不大,本题注意衡量一个国家的石油化工水平的物质为乙烯,此为解答该题的关键之处,注意把握常见有机物的官能团和性质.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
 (2011?新余二模)化学--选修物质结构与性质
(2011?新余二模)化学--选修物质结构与性质
 已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
 已知单质A、B、C、D有如下的反应关系.其中A 在B中燃烧时,火焰呈苍白色; C在B中燃烧时生成棕黄色的烟,E的水溶液呈蓝绿色,G是一种黑色固体.
已知单质A、B、C、D有如下的反应关系.其中A 在B中燃烧时,火焰呈苍白色; C在B中燃烧时生成棕黄色的烟,E的水溶液呈蓝绿色,G是一种黑色固体.