题目内容
V mL Al2(SO4)3溶液中含有Al3+a g,取0.5V mL溶液稀释到4V mL,则稀释后溶液中S042-的物质的量浓度是( )
分析:根据n=
计算ag Al3+的物质的量,进而计算0.5VmL溶液中Al3+的物质的量,根据电荷守恒可知2n(SO42-)=3n(Al3+),溶液稀释为4VmL,溶液中SO42-的物质的量不变,再根据c=
计算稀释后溶液SO42-的物质的量浓度.
| m |
| M |
| n |
| V |
解答:解:ag Al3+的物质的量为
=
mol,
故0.5VmL溶液中Al3+的物质的量为
mol×
=
mol,
根据电荷守恒可知2n(SO42-)=3n(Al3+),故0.5VmL溶液中SO42-的物质的量为
mol×
=
mol,
0.5VmL溶液稀释到4V mL,则稀释后溶液SO42-的物质的量浓度为
=
mol/L,
故选B.
| ag |
| 27g/mol |
| a |
| 27 |
故0.5VmL溶液中Al3+的物质的量为
| a |
| 27 |
| 0.5V mL |
| V mL |
| a |
| 54 |
根据电荷守恒可知2n(SO42-)=3n(Al3+),故0.5VmL溶液中SO42-的物质的量为
| a |
| 54 |
| 3 |
| 2 |
| a |
| 36 |
0.5VmL溶液稀释到4V mL,则稀释后溶液SO42-的物质的量浓度为
| ||
| 4V×10-3L |
| 125a |
| 18V |
故选B.
点评:本题考查物质的量浓度的有关计算,难度不大,注意对公式的理解与灵活运用,属于字母型计算,容易计算出问题.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
 V mol溶液稀释到4V mL,
V mol溶液稀释到4V mL, mol/L
B.
mol/L
B. mol/L
C.
mol/L
C. mol/L
D.
mol/L
D.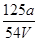 mol/L
mol/L