题目内容
下图是一甲醇(CH3OH)燃料电池的化学原理示意图,下列判断不正确的是
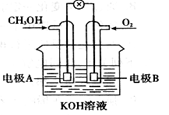
- A.电极A为电池负极
- B.电极B表面上发生还原反应
- C.工作一段时间溶液pH保持不变
- D.燃料电池工作时不会出现火焰
C
在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。所以在甲醇燃料电池中,甲醇在负极通入,氧气在正极通入,即A是负极,B是正极。由于氧气和甲醇不直接接触,不可能产生火焰,D不正确。因为反应后会生产碳酸钾,消耗氢氧化钾,因此溶液的碱性降低,选项C是错误的。答案选C。
在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。所以在甲醇燃料电池中,甲醇在负极通入,氧气在正极通入,即A是负极,B是正极。由于氧气和甲醇不直接接触,不可能产生火焰,D不正确。因为反应后会生产碳酸钾,消耗氢氧化钾,因此溶液的碱性降低,选项C是错误的。答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(10分)二甲基亚砜有消炎止痛、镇静等作用。甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫醚(CH3—S—CH3),甲硫醚再与NO2反应制取二甲基亚砜 ( ),有关反应如下:
),有关反应如下:
反应① 2CH3OH(l)+H2S(g)=(CH3)2S(l) +2H2O(l) △H=―akJ·mol-1
反应② (CH3)2S(l)+NO2(g)=(CH3)2SO(l)+NO(g) △H=-bkJ··mol-1
反应③ 2NO(g)+O2(g)=2NO2(g) △H=-ckJ·mol-1
(1)写出用甲硫醚直接和氧气反应制取二甲基亚砜的热化学反应方程式
___________________________________________________, (2)能说明反应2CH3OH(l)+H2S(g) (CH3)2S(l) +2H2O(l)达平衡状态的是____________ 。
(2)能说明反应2CH3OH(l)+H2S(g) (CH3)2S(l) +2H2O(l)达平衡状态的是____________ 。
| A.v(CH3OH) =" 2v(H2S)" |
| B.恒容容器中,体系的压强不再改变 |
| C.恒容容器中,体系中气体的密度不再改变 |
D.恒容容器中,气体的摩尔质量不 再改变 再改变 |
(4)N2O5是一种新型绿色硝化剂,其制备方法有以下两种。
方法一:4NO2(g)+O2(g) =2N2O5(g)
 ;△H=-56.76 KJ·mol-1
;△H=-56.76 KJ·mol-1 常温下,该反应能逆向自发进行,则逆向反应的△S __________ 0(填“>、<”或“=”)
方法二:用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5。工作原理如下图:

硼氢化钠燃料电池的正极反应式________________________。



 ②含有对位二取代苯环
②含有对位二取代苯环
 ),有关反应如下:
),有关反应如下: (2)能说明反应2CH3OH(l)+H2S(g)
(CH3)2S(l) +2H2O(l)达平衡状态的是____________
。
(2)能说明反应2CH3OH(l)+H2S(g)
(CH3)2S(l) +2H2O(l)达平衡状态的是____________
。
 CH3OH(g)。
CH3OH(g)。
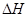 0(填“>”、“<”或“=”)。
0(填“>”、“<”或“=”)。