题目内容
| |||||||||||||||||||||||||||||||
解析:
(1) |
10 g |
(2) |
高于 调节平衡螺丝使之平衡 32.6 g |
(3) |
|
(4) |
①③④②⑤ |
(5) |
m(NaOH)=M·n=40 g/mol×500×10-3 L×0.5 mol/L=10 g. 刻度盘的指针偏向哪方,哪方就重,左边托盘高于右边托盘,这时应先往左盘添加药品.天平精确到0.1 g,所以称量结果只能为32.6 g,在称量物品时,砝码的选择是由大到小.而溶液的配制过程为:计算→称量→溶解→转移→定容→装瓶→贴签. 配制出的溶液浓度小于所要求的原因,可能是:①使用滤纸称量NaOH,因为NaOH吸收空气中的水和CO2,从而使实际使用的NaOH质量小了;②溶解后的烧杯未经多次洗涤,从而使溶质残留在烧杯中;③定容时仰视,此时液面已经超过了刻度线.而容量瓶中是否有蒸馏水则不影响结果. |

 名校课堂系列答案
名校课堂系列答案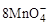 +5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O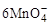 +5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O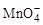 +______Fe2++______H+=______Mn2++______Fe3++______H2O
+______Fe2++______H+=______Mn2++______Fe3++______H2O