题目内容
冰晶石(化学式为Na3AlF6)的晶体结构单元如下图所示,已知冰晶石熔融时电离方程式为:Na3AlF6====3Na++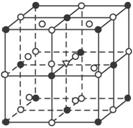
·位于大立方体的顶点和面心
。位于大立方体的12条棱的中点和8个小立方体的体心
那么大立方体的体心处?所代表的粒子应为( )
A.Na+ B.Al3+ C.F- D. ![]()
解析:①从电离方程式看出,Al元素和F元素均以![]() 整体的形式出现。
整体的形式出现。
②从晶体结构看,由于阴、阳一定是交替结构,所以,一定是阳离子。
③在晶体结构中·的数目:顶点取其![]() ,面心取其
,面心取其![]() ,则共有:8×
,则共有:8×![]() +6×
+6×![]() =4。
=4。
④在晶体结构中○的数目:棱中点取其![]() ,体心点取其1,则○共有:12×
,体心点取其1,则○共有:12×![]() +8×1=12。
+8×1=12。
⑤由于·的数目∶○的数目=1∶3,故·是![]() ,○是Na+。
,○是Na+。
答案:A

练习册系列答案
相关题目
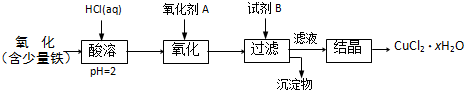
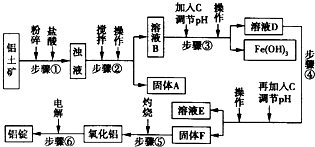
生活中常使用的铝合金中的铝来自于电解熔融氧化铝.用于工业电解的氧化铝要求其纯度不得低于98.2%,而天然铝土矿中的氧化铝含量为50%~70%,杂质主要为SiO2、Fe2O3、CaO、MgO、Na2O等.工业生产铝锭的工艺流程示意图如下所示:

一些难溶物开始沉淀和完全沉淀的pH如表所示:
请回答下列问题:
(1)加入盐酸时,氧化铝与盐酸发生反应的离子方程式为______.
(2)步骤②③④中操作的名称为______.
(3)固体A的化学式为______;物质C的化学式为______:溶液中的Na+、Ca2+、Mg2+是在步骤______中除去的.
(4)步骤③中调节溶液pH的数值范围为______,步骤④中调节溶液pH的数值范围为______.
(5)步骤⑥中发生反应的化学方程式为______冰晶石4Al+3O2↑

一些难溶物开始沉淀和完全沉淀的pH如表所示:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀pH(离子初始浓度为0.01mol、L) | 4 | 2.3 | 10.4 |
| 完全沉淀pH(离子浓度<10-5mol/L) | 5.2 | 4.1 | 12.4 |
(1)加入盐酸时,氧化铝与盐酸发生反应的离子方程式为______.
(2)步骤②③④中操作的名称为______.
(3)固体A的化学式为______;物质C的化学式为______:溶液中的Na+、Ca2+、Mg2+是在步骤______中除去的.
(4)步骤③中调节溶液pH的数值范围为______,步骤④中调节溶液pH的数值范围为______.
(5)步骤⑥中发生反应的化学方程式为______冰晶石4Al+3O2↑
 (1)如图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种.图中●、○分别指代哪种粒子
(1)如图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种.图中●、○分别指代哪种粒子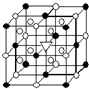 A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子
A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子