��Ŀ����
 ��ҵ������N2��H2���Ժϳ�NH3��NH3�ֿ��Խ�һ���Ʊ�������N2H4���ȣ�
��ҵ������N2��H2���Ժϳ�NH3��NH3�ֿ��Խ�һ���Ʊ�������N2H4���ȣ���1���������N2H4��ȼ�ϣ�N2O4������������֪��
N2��g��+2O2��g���T2NO2��g����H=67.7kJ?mol-1
N2H4��g��+O2��g���TN2��g��+2H2O��g����H=-534.0kJ?mol-1
NO2��g��?
| 1 | 2 |
��д����̬��������̬������������ȼ�����ɵ�������̬ˮ���Ȼ�ѧ����ʽ��
��2������--����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%��30%���ⰱ������Һ���õ�طŵ�ʱ�������ĵ缫��ӦʽΪ
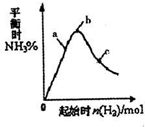
��3����300��ʱ���ı���ʼ��Ӧ�������������ʵ����Է�ӦN2��g��+2H2��g��?2NH3��g����H��0��Ӱ����ͼ��ʾ��
������ͼ�л���400��ʱ��Ӧ��ͼ��
����a��b��c�����У�H2��ת������ߵ���
��������1�����ݸ�˹���ɣ�����֪�Ȼ�ѧ����ʽ���Ժ��ʵ�ϵ�������ʵ��ļӼ�����Ӧ��Ҳ������Ӧ��ϵ��������Ӧ�ļӼ���
��2��ȼ�ϵ�ص�������ȼ�Ͽ����е������õ��ӷ�����ԭ��Ӧ����O2 +4e-+2H2O=4OH-��
��3�����¶ȶԻ�ѧƽ���ƶ���Ӱ�죬�����¶Ȼ�ѧƽ�����淴Ӧ�ƶ�������ƽ��ٷֺ������٣�
�ڻ�ѧƽ��ת���ʵĿ��飬�Զ������ʲμӷ�Ӧ���ı�����һ�����ʣ�����һ����ת���ʵ�Ӱ�죮
��2��ȼ�ϵ�ص�������ȼ�Ͽ����е������õ��ӷ�����ԭ��Ӧ����O2 +4e-+2H2O=4OH-��
��3�����¶ȶԻ�ѧƽ���ƶ���Ӱ�죬�����¶Ȼ�ѧƽ�����淴Ӧ�ƶ�������ƽ��ٷֺ������٣�
�ڻ�ѧƽ��ת���ʵĿ��飬�Զ������ʲμӷ�Ӧ���ı�����һ�����ʣ�����һ����ת���ʵ�Ӱ�죮
����⣺��1����֪����N2��g��+2O2��g��=2NO2��g����H=+67.7kJ?mol-1
��N2H4��g��+O2��g��=N2��g��+2H2O��g����H=-534.0kJ?mol-1
��NO2��g��?
N2O4��g����H=-26.35kJ?mol-1
���ݸ�˹���ɣ��ڡ�2-��-�ۡ�2��2N2H4��g��+N2O4��g��=3N2��g��+4H2O��g����
�ʡ�H=2����-534.0kJ?mol-1��-67.7kJ?mol-1-2����-26.35kJ?mol-1��=-1083kJ?mol-1��
���Ȼ�ѧ����ʽΪ2N2H4��g��+N2O4��g��=3N2��g��+4H2O��g����H=-1083kJ?mol-1��
�ʴ�Ϊ��2N2H4��g��+N2O4��g��=3N2��g��+4H2O��g����H=-1083kJ?mol-1��
��2��ȼ�ϵ�ص�������ȼ�Ͽ����е������õ��ӷ�����ԭ��Ӧ��1mol�����õ�4mol���ӣ����2mol��������4molOH-���ʴ�Ϊ��O2 +4e-+2H2O=4OH-��
��3��������Ӧ�Ƿ��ȷ�Ӧ���������¶ȣ�ƽ�����淴Ӧ�����ƶ������Ե��¶�����ʱ�����ĺ������ͣ���ͼ��Ϊ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���ڿ��淴ӦA+B?C������һ�ַ�Ӧ��A���������������һ�ַ�Ӧ��B��ת���ʣ���A������ת���ʷ������ͣ�������������ԽС��H2��ת������ߣ��ʴ�Ϊ��a��
��N2H4��g��+O2��g��=N2��g��+2H2O��g����H=-534.0kJ?mol-1
��NO2��g��?
| 1 |
| 2 |
���ݸ�˹���ɣ��ڡ�2-��-�ۡ�2��2N2H4��g��+N2O4��g��=3N2��g��+4H2O��g����
�ʡ�H=2����-534.0kJ?mol-1��-67.7kJ?mol-1-2����-26.35kJ?mol-1��=-1083kJ?mol-1��
���Ȼ�ѧ����ʽΪ2N2H4��g��+N2O4��g��=3N2��g��+4H2O��g����H=-1083kJ?mol-1��
�ʴ�Ϊ��2N2H4��g��+N2O4��g��=3N2��g��+4H2O��g����H=-1083kJ?mol-1��
��2��ȼ�ϵ�ص�������ȼ�Ͽ����е������õ��ӷ�����ԭ��Ӧ��1mol�����õ�4mol���ӣ����2mol��������4molOH-���ʴ�Ϊ��O2 +4e-+2H2O=4OH-��
��3��������Ӧ�Ƿ��ȷ�Ӧ���������¶ȣ�ƽ�����淴Ӧ�����ƶ������Ե��¶�����ʱ�����ĺ������ͣ���ͼ��Ϊ
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�����ڿ��淴ӦA+B?C������һ�ַ�Ӧ��A���������������һ�ַ�Ӧ��B��ת���ʣ���A������ת���ʷ������ͣ�������������ԽС��H2��ת������ߣ��ʴ�Ϊ��a��
���������⿼�����ø�˹���ɽ��з�Ӧ�ȼ��㡢ȼ�ϵ�ص缫��Ӧ����ʽ����д���Լ���ѧƽ��ԭ���Ŀ��飬Ҳ������������ѧ�α�֪ʶ�ܹ�ѧ�����ã����������ǿ���Ѷ��еȣ�ע��缫��Ӧʽ����д��Ϊ�״��㡢�ѵ㣮

��ϰ��ϵ�д�
 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
�����Ŀ
����Ӧ�ò��漰������ԭ��Ӧ���ǣ�������
| A����ҵ������N2��H2�ϳɰ���ʵ���˹��̵� | B��ʵ������NH4Cl��Ca��0H��2�Ʊ�NH3 | C����FeCl3��Һ��Ϊ����ʴҺ����ʴ��·ͭ�� | D����Na2O2��DZˮͧ�Ĺ����� |
