题目内容
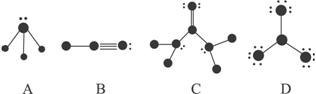
下列结构图中●代表原子停数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未形成共价键的最外层电子,短线代表价键,如:F2
根据各图所示的结构特点,写出相应分子的化学式:
A:________________;
B:________________;
C:________________;
D:________________。
答案:
解析:
解析:
| 解析:此题是让考生看图识分子。考生通过分析1~10号元素原子的化合价和化学键后,便能顺利辨认出这些分子。
A图,显然是NH3。第一,它是一个三角锥型分子;第二,它有一对电子未参加成键,3个价电子用于形成3个单键,最外层应有5个电子,必为N原子。而与N相连的原子只有一个价电子,故只可以是H原子。 B图是H—C≡N;这是因为第一,它是直线型分子; 第二,中间一个原子化合价为4,所以是C,左边原子化合价为1,且只有一个价电子,故为H,而右边原子显然是N。
C图是H2N—C—NH2。从图可看出,顶上的原子是O原子,它用2个价电子与C形成两对共用电子对。左、右两边与C相连的显然是N原子,同理与N相连的两个只含1个价电子的原子显然是H原子。 D图是BF3。在1~10号元素中价电子为7的只有F原子,每个F各用一个价电子与中间原子形成单键,而中间一个原子只有3个价电子,应该是B原子,故该分子是平面三角形的BF3。 答案:NH3 HCN CO(NH2)2 BF3 点评:考生在书上读到的、在黑板上见到的大多数分子、离子的表达式,只是平面的、无结构的化学符号,然而分子、离子都是实体,它实际上是三维的,而且它们的许多性质通常同时受电子结构和空间效应两方面的制约。考生对分子的电子结构了解不多,对分子、离子的立体结构观念更薄弱,该题试图引导考生从最早的学习阶段开始就注意它们的电子结构和几何构型。 本题测试了考生接受新信息,结合已有知识,运用于解题的自学能力、应变能力、排除流行误解相信自己判断的定向能力。
|

练习册系列答案
相关题目



 ,硝基甲烷
,硝基甲烷 ,写出三硝酸甘油酯的结构式:_________。
,写出三硝酸甘油酯的结构式:_________。