题目内容
常温下,将 pH和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,pH随溶液体积变化如下图,下列有关叙述正确的是
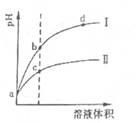
- A.曲线I为醋酸稀释时pH值变化曲线
- B.a点时,若都加入相同大小的锌粒,此时与盐酸反应的速率大
- C.a点时,若都加入足量的锌粒,最终与醋酸反应产生的氢气多
- D.b点溶液中水的电离程度比c点溶液中水的电离程度大
试题分析:稀释能促进弱酸电离平衡向电离方向移动,则稀释相同倍数时,盐酸pH的变化程度大于醋酸,所以图中I表示盐酸,II表示醋酸,故A错误;Zn+2H+=Zn2++H2↑,a点时盐酸和醋酸的pH相同,则c(H+)相同,因此反应速率相等,故B错误;a点时盐酸和醋酸的c(H+)相同,但前者的电离程度大于后者,则c(HCl)<c(CH3COOH),因此n(HCl)<n(CH3COOH),所以醋酸与足量锌粒反应放出的氢气多,故C正确;H2O
 H++OH―,b点的pH大于c点的pH,则b点的c(H+)小于c点的c(H+),酸电离出的c(H+)越大,水的电离平衡越向左移动,水的电离程度越小,则b点水的电离程度大于c点,故D正确。
H++OH―,b点的pH大于c点的pH,则b点的c(H+)小于c点的c(H+),酸电离出的c(H+)越大,水的电离平衡越向左移动,水的电离程度越小,则b点水的电离程度大于c点,故D正确。考点:考查强弱电解质、溶液的pH、弱酸的电离平衡、水的电离平衡、化学反应速率的大小比较等。

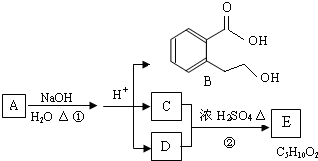
(18分)下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。
根据下图回答问题:
(1)C分子中的官能团名称是: ______________;下列反应中,化合物B不能发生的反应是 (填字母序号):
a 加成反应 b取代反应 c消去反应 d酯化反应 e水解反应 f加聚反应。
(2)反应②的化学方程式是 ________。
(3)A的结构简式是 __________________ 。
(4)同时符合下列三个条件的B的同分异构体的数目有 个。
Ⅰ.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式
(5)常温下,将C溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液pH如下表:
| 实验编号 | C物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
| m | 0.1 | 0.1 | pH=9 |
| n | 0.2 | 0.1 | pH<7 |
从m组情况分析,用离子方程式表示该溶液pH=9的原因 。
n组混合溶液中离子浓度由大到小的顺序是 。
28.(15分)下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。
根据上图回答问题:
(1)C分子中的官能团名称是______________;化合物B不能发生的反应是 (填字母序号):
a 加成反应 b取代反应 c消去反应 d酯化反应 e水解反应 f 置换反应
(2)反应②的化学方程式是___________ _。
(3)试分析反应②加热的原因。
Ⅰ、 。;
Ⅱ、 。。
(4)A的结构简式是__________________ 。
(5)同时符合下列三个条件的B的同分异构体的数目有 个。
Ⅰ.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3 溶液发生显色反应。
写出其中任意一个同分异构体的结构简式 。
(6)常温下,将C溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | C物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
| m | 0.1 | 0.1 | pH=9 |
| n | 0.2 | 0.1 | pH<7 |
从m组情况分析,所得混合溶液中由水电离出的c(OH-)= mol·L-1。
n组混合溶液中离子浓度由大到小的顺序是 ___________。
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。

根据上图回答问题:
(1)C分子中的官能团名称是 ______________;化合物B不能发生的反应是 (填字母序号):
a 加成反应 b取代反应 c消去反应 d酯化反应 e水解反应 f 置换反应
(2)反应②的化学方程式是_________________ _。
(3)反应②实验中加热的目的是:
Ⅰ、 。;
Ⅱ、 。。
(4)A的结构简式是 __________________ 。
(5)同时符合下列三个条件的B的同分异构体的数目有 个。
Ⅰ.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3 溶液发生显色反应。
写出其中任意一个同分异构体的结构简式 。
(6)常温下,将C溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH
如下表:
| 实验编号 | C物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
| m | 0.1 | 0.1 | pH=9 |
| n | 0.2 | 0.1 | pH<7 |
从m组情况分析,所得混合溶液中由水电离出的c(OH-)= mol·L-1。
n组混合溶液中离子浓度由大到小的顺序是 。

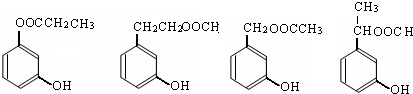 写出四者之一即可
写出四者之一即可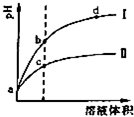 常温下,将PH值和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,PH但随溶液体 积变化如图,下列有关叙述正确的是( )
常温下,将PH值和体积都相同的盐酸和醋酸溶液分别加蒸馏水稀释,PH但随溶液体 积变化如图,下列有关叙述正确的是( )