题目内容
(12分)氨在国民经济中占有重要地位。
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
①工业合成氨的热化学方程式是_______。
②若起始时向容器内放入2 mol N2和6 mol H2,达平衡后放出的热量为Q,则Q(填“>”、“<”或“=”)_______184.4 kJ。
③已知:

1 mol N-H键断裂吸收的能量约等于_______kJ。
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O
(l),该反应的平衡常数和温度关系如下:
CO(NH2)2 (l) + H2O
(l),该反应的平衡常数和温度关系如下:
|
T / ℃ |
165 |
175 |
185 |
195 |
|
K |
111.9 |
74.1 |
50.6 |
34.8 |
①焓变ΔH(填“>”、“<”或“=”)_______0。
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)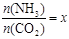 ,下图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是_______。
,下图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是_______。

③上图中的B点处,NH3的平衡转化率为_______。
(1)①

② < ③391
(2)① < ②c(NH3)增大,平衡正向移动 ③32%
【解析】
试题分析:(1)合成氨工业中每产生2 mol NH3,放出92.2
kJ热量。根据定量关系可以得到①工业合成氨的热化学方程式是①
 ;由于该反应是可逆反应所以2 mol N2和6 mol H2完全反应理论上可以放出184.4
kJ热量,但是实际中得到的只能比184.4 kJ少所以②若起始时向容器内放入2 mol N2和6 mol H2,达平衡后放出的热量为Q<184.4 kJ。
;由于该反应是可逆反应所以2 mol N2和6 mol H2完全反应理论上可以放出184.4
kJ热量,但是实际中得到的只能比184.4 kJ少所以②若起始时向容器内放入2 mol N2和6 mol H2,达平衡后放出的热量为Q<184.4 kJ。
③已知:

所以由反应热的计算公式可得6 mol N-H键能—(1 mol N-N键能+3 mol H-H键能)=92.2kj
所以1 mol N-H键断裂吸收的能量约等于391kJ。
(2)由该反应的平衡常数和温度关系
|
T / ℃ |
165 |
175 |
185 |
195 |
|
K |
111.9 |
74.1 |
50.6 |
34.8 |
可以看到温度越高,平衡向吸热方向移动,K越小,平衡向逆反应方向移动,即逆反应方向就是吸热方向所以正反应方向为放热反应,所以①焓变ΔH<0。
② 2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O
(l)增加NH3的浓度,平衡会向正反应方向移动,所以CO2平衡转化率会增大
CO(NH2)2 (l) + H2O
(l)增加NH3的浓度,平衡会向正反应方向移动,所以CO2平衡转化率会增大
2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O
(l)
CO(NH2)2 (l) + H2O
(l)
起始量物质的量: 4x x 0 0
变化量物质的量: 2y y y y
平衡量物质的量: 4x-2y x-y y y
CO2平衡转化率a=y/x=64%
所以③上图中的B点处,NH3的平衡转化率=2y/4x=32%
考点:热化学方程式的书写反应热的计算化学平衡
点评:会用化学键计算反应热,会用三行式进行化学平衡的计算,能熟练运用化学平衡常数和温度的变化分析正逆反应的吸放热情况。“三行式”即:第一行表示的是物质开始反应的量,第二行表示的是物质反应的量,第三行表示的是物质反应后的量。

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案

 2NH3的△H
2NH3的△H