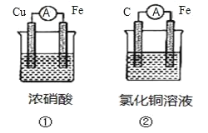
题目内容
【题目】KI溶液在酸性条件下能与氧气反应。现有以下实验记录:
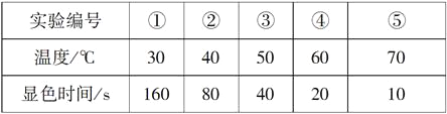
回答下列问题:
(1)该反应的离子方程式为_____________________________________。
(2)该实验的目的是__________________________________。
(3)实验试剂除了1 mol·L-1KI溶液、0.1 mol·L-1H2SO4溶液外,还需要的试剂是________,实验现象为_____________________________。
(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是________(填字母)。
A.温度
B.试剂的浓度
C.试剂的用量(体积)
D.试剂添加的顺序
(5)由上述实验记录可得出的结论是_________________________。
(6)若要进行溶液酸性大小对反应速率的影响的探究实验,你会采取的措施是_________。
【答案】4H++4I-+O2===2I2+2H2O 探究温度对反应速率的影响 淀粉溶液 无色溶液变蓝 CD 每升高10 ℃,反应速率增大约2倍 保持其他实验条件不变,采用不同浓度的硫酸溶液进行对比实验
【解析】
(1)根据反应物和生成物书写离子方程式;
(2)根据表中数据分析该实验目的;
(3)为测定显色时间,产物中有碘单质生成,还需要的试剂是淀粉溶液,据此判断;
(4)设计实验必须保证其他条件不变,只改变一个条件,才能得到准确的结论,结合表中数据分析;
(5)结合表中数据分析结论;
(6)若要进行酸性对反应速率的影响的探究实验,采用不同浓度的硫酸溶液进行对比实验。
(1)氧气在酸性溶液中氧化碘离子生成单质碘,同时还有水生成,该反应的离子方程式为4H++4I-+O2=2I2+2H2O;
(2)根据表中数据分析,该实验目的是探究温度对反应速率的影响;
(3)为测定显色时间,产物中有碘单质生成,因此还需要的试剂是淀粉溶液,实验现象为无色溶液变蓝色;
(4)设计实验必须保证其他条件不变,只改变一个条件,才能得到准确的结论,因此根据以上分析可知还必须控制不变的是试剂的用量(体积)和试剂添加的顺序,故答案为CD;
(5)通过表中数据分析可得出的结论是每升高10℃,反应速率增大约2倍;
(6)若要进行酸性对反应速率的影响的探究实验,你会采取的措施是保持其他实验条件不变,采用不同浓度的硫酸溶液进行对比实验。

【题目】原子序数依次增大的短周期主族元素X、Y、Z、W、R,其中X、Y两种元素的核电荷数之差等于它们的原子最外层电子数之和;Y、Z位于相邻主族;Z是地壳中含量最高的元素;X、W是同主族元素。上述五种元素两两间能形成四种常见的化合物甲、乙、丙、丁,这四种化合物中原子个数比如下表:
甲 | 乙 | 丙 | 丁 | |
化合物中各元素原子个数比 |
|
|
|
|
(1)写出下列元素符号:Y_____________,Z_______________,W_____________,R________________。
(2)写出下列化合物的电子式:乙_______________,丙__________________。
(3)向甲的水溶液中加入丁,有淡黄色沉淀生成,请写出反应的化学方程式:__________________。
(4)甲和乙反应能放出大量的热,同时生成两种无污染的物质,请写出该反应的化学方程式:______________________________。