题目内容
把一块镁铝合金投入到1 mol·L-1盐酸中,待合金完全溶解后,再往溶液里加入1 mol·L-1NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示。下列说法中错误的是
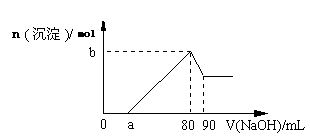
- A.盐酸的体积为80 mL
- B.a的取值范围为0 < a<50
- C.n (Mg2+) < 0.025 mol
- D.当a值为30时,b值为0.01
D
当沉淀达到最高值时,生成氯化钠是0.08mol,所以盐酸的物质的量也是0.08mol,其体积是80ml,A正确。溶解氢氧化铝消耗氢氧化钠是10mol,则生成氢氧化铝需要氢氧化钠是30ml,所以a一定小于50ml,B正确。如果镁离子是0.025mol,则生成氢氧化镁需要氢氧化钠的体积就是50ml,而生成氢氧化钠需要30mol,显然80-a不可能等于80,所以C正确。当a值为30时,生成氢氧化镁消耗的氢氧化钠(80-30-30)ml=20mol,所以生成氢氧化镁是0.01mol,因此沉淀一共是0.01mol+0.01mol=0.02mol,D不正确。答案选D。
当沉淀达到最高值时,生成氯化钠是0.08mol,所以盐酸的物质的量也是0.08mol,其体积是80ml,A正确。溶解氢氧化铝消耗氢氧化钠是10mol,则生成氢氧化铝需要氢氧化钠是30ml,所以a一定小于50ml,B正确。如果镁离子是0.025mol,则生成氢氧化镁需要氢氧化钠的体积就是50ml,而生成氢氧化钠需要30mol,显然80-a不可能等于80,所以C正确。当a值为30时,生成氢氧化镁消耗的氢氧化钠(80-30-30)ml=20mol,所以生成氢氧化镁是0.01mol,因此沉淀一共是0.01mol+0.01mol=0.02mol,D不正确。答案选D。

练习册系列答案
相关题目
把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图A所示.下列说法中不正确的是( )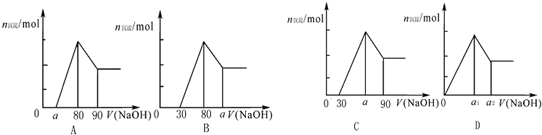

| A、a的取值范围为0≤a<50 | ||
B、
| ||
| C、若将关系图改为B图时,则a的取值范围为80<a<90 | ||
| D、若将关系图改为C图时,则a的取值范围为75<a<90 |
把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图A所示.下列说法不正确的是( )
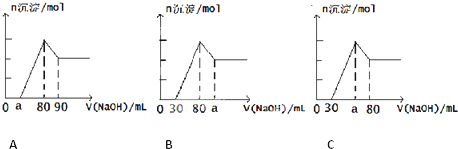

| A、A图中a的取值范围为0≤a<50 | ||
B、A图中
| ||
| C、若将关系图改为B图时,则a的取值范围为80<a<90 | ||
| D、若将关系图改为C图时,则a的取值范围为67.5<a<80 |

 (2011?抚顺二模)把一块镁铝合金投入到1mol?L-1 盐酸中,待合金完全溶解后,再往溶液里加入1mol?L-1 NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示.下列说法中错误的是( )
(2011?抚顺二模)把一块镁铝合金投入到1mol?L-1 盐酸中,待合金完全溶解后,再往溶液里加入1mol?L-1 NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示.下列说法中错误的是( ) 把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,再往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示.下列说法中错误的是( )
把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,再往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示.下列说法中错误的是( )