��Ŀ����
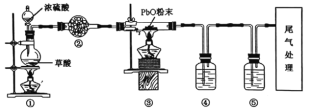
����Ŀ��ʵ�����ò�����Ũ���ᷴӦ�Ʊ�CO,��ԭ�����£�H2C2O4![]() CO��+CO2��+H2O��ij������ͬѧ���ʵ��̽��CO��ԭ����Ǧ(��ɫ��ĩ)��������������(��֪CO��ʹ������Һ������ɫ����),װ����ͼ��ʾ��
CO��+CO2��+H2O��ij������ͬѧ���ʵ��̽��CO��ԭ����Ǧ(��ɫ��ĩ)��������������(��֪CO��ʹ������Һ������ɫ����),װ����ͼ��ʾ��
����˵����ȷ���ǣ� ��
A. �ڡ��ܡ������Լ�����Ϊ��ʯ�ҡ�������Һ������ʯ��ˮ
B. ����������������������������ʱ˵�����п������ž�
C. ʵ�����ʱ,��Ϩ��ٴ��ƾ���,��Ϩ��۴��ƾ���
D. ʵ������й۲쵽�۲������л�ɫ��ĩ��ɰ�ɫ��ĩ
���𰸡�B
��������
A.װ���Т���Ҫ����CO��CO2��H2O������Ϊ��ʯ�����ڳ�ȥCO2��H2O �����з�����Ӧ��PbO+CO![]() CO2+Pb�������ó���ʯ��ˮ���鲢��ȥ��Ӧ�����ɵ�CO2��������������Һ����װ�����Ƿ������CO�����Т������������Լ�����Ϊ��ʯ�ҡ�����ʯ�ҡ�ˮ������Һ����A����B.������������������������������ʱ˵�����п������ž�����B��ȷ��C.ʵ�����ʱ,��Ϩ��۴��ƾ���,��Ϩ��ٴ��ƾ��ƣ��Է�������������C����D.һ��������ֳ�����ɫ���������ڷ�ĩ״Ϊ�Һ�ɫ����D����ѡB��
CO2+Pb�������ó���ʯ��ˮ���鲢��ȥ��Ӧ�����ɵ�CO2��������������Һ����װ�����Ƿ������CO�����Т������������Լ�����Ϊ��ʯ�ҡ�����ʯ�ҡ�ˮ������Һ����A����B.������������������������������ʱ˵�����п������ž�����B��ȷ��C.ʵ�����ʱ,��Ϩ��۴��ƾ���,��Ϩ��ٴ��ƾ��ƣ��Է�������������C����D.һ��������ֳ�����ɫ���������ڷ�ĩ״Ϊ�Һ�ɫ����D����ѡB��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ����̽��������ˮ�ɷּ����ʵ�ʵ���У��������з������������ܵó���Ӧ���۵���
���� | ���� | ���� | |
A | �۲���ˮ��ɫ | ��ˮ�ʻ���ɫ | ��ˮ�к�Cl2 |
B | ��NaHCO3��Һ�м���������ˮ | ����ɫ������� | ��ˮ�к�HClO |
C | ���ɫֽ���ϵμ���ˮ | ��ɫֽ����ɫ | ��ˮ����Ư���� |
D | ��FeCl2��Һ�еμ���ˮ | ��Һ����ػ�ɫ | ��ˮ���������� |
A. A B. B C. C D. D