题目内容
15.如图是实验室制溴苯的装置图,下列说法正确的是( )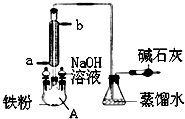
| A. | 仪器A左上侧的分液漏斗中加入的是苯和溴水 | |
| B. | 仪器A的名称叫蒸馏烧瓶 | |
| C. | NaOH溶液的主要作用是除去反应后溶解在溴苯中的溴 | |
| D. | 碱石灰作用是防止空气中水蒸气进入反应体系 |
分析 A.苯与溴水不反应;
B.依据仪器图型判断其名称;
C.溴能够与氢氧化钠发生反应,被氢氧化钠吸收;
D.尾气中含有HBr与挥发出的Br2,直接排放会污染大气.
解答 解:A.苯与液溴反应生成溴苯与溴水不反应,故仪器A左上侧的分液漏斗中加入的是苯和液溴,故A错误;
B.器A的名称叫三颈烧瓶,故B错误;
C.溴能够与氢氧化钠发生反应,被氢氧化钠吸收,故C正确;
D.尾气中含有HBr与挥发出的Br2,直接排放会污染大气,碱石灰作用是吸收HBr与Br2,防止污染空气,故D错误;
故选:C.
点评 本题考查实验室溴苯的制取,把握物质的性质、反应原理及实验装置的作用为解答的关键,题目难度中等.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
14. 常温下,向10mL 0.1mol•L-1的HCl溶液中逐滴加入0.1mol•L-1的NH3•H2O溶液,其pH逐渐增大,图中a,b,c三点的pH为实验所测得.下列有关说法中一定错误的是( )
常温下,向10mL 0.1mol•L-1的HCl溶液中逐滴加入0.1mol•L-1的NH3•H2O溶液,其pH逐渐增大,图中a,b,c三点的pH为实验所测得.下列有关说法中一定错误的是( )
 常温下,向10mL 0.1mol•L-1的HCl溶液中逐滴加入0.1mol•L-1的NH3•H2O溶液,其pH逐渐增大,图中a,b,c三点的pH为实验所测得.下列有关说法中一定错误的是( )
常温下,向10mL 0.1mol•L-1的HCl溶液中逐滴加入0.1mol•L-1的NH3•H2O溶液,其pH逐渐增大,图中a,b,c三点的pH为实验所测得.下列有关说法中一定错误的是( )| A. | 水的电离程度先增大后减小 | |
| B. | 当pH=7时,所加NH3•H2O溶液的体积大于10mL | |
| C. | 当7<pH<9时,溶液中c(NH4+)>c(Cl-) | |
| D. | 继续滴加0.1mol•L-1的NH3•H2O溶液,溶液的pH最终可以变化至13 |
6.某元素X最高价含氧酸的分子量为98,且X的氢化物的分子式不是H2X,则下列说法正确的是( )
| A. | X的最高化合价为+4 | |
| B. | X是第二周期VA族元素 | |
| C. | X是第二周VIA族元素 | |
| D. | X的最高价含氧酸的分子式可表示为H3XO4 |
3.纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.
(1)A和B的单质单位质量的燃烧热大,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
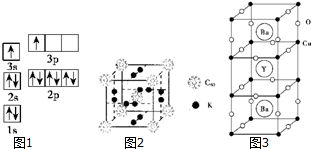
①某同学根据上述信息,某同学推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了能量最低原理.
②根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为直线形.A原子杂化类型是sp.
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.
①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认识C60的熔点高于金刚石,你认为是否正确不正确理由是因为C60构成的晶体是分子晶体,影响分子晶体熔点的作用是分子间作用力;而金刚石构成的晶体是原子晶体,影响原子晶体熔点的作用是原子间共价键,共价键作用大大与分子间作用力,因此金刚石的熔点高于C60.
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.该物质的K原子和C60分子的个数比为3:1.晶胞中每个C60分子周围与之等距离且最近的C60分子数是6.
③继C60后,科学家又合成了Si60、N60;C、Si、N原子电负性由大到小的顺序是N>C>Si.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为30.
(3)1986年,瑞士两位科学家发现一种性能良好的金属氧化物超导体,使超导工作取得突破性进展,为此两位科学家获得了1987年的Nobel物理学奖.其晶胞结构如图3.
①根据图示晶胞结构,推算晶体中Y、Cu、Ba和O原子个数比,其化学式YBa2Cu3O7.
②已知该化合物中各元素的化合价Y为+3价,Ba为+2价,Cu为+2价和Cu为+3价,根据①所推出的化合物的组成,试计算化合物中这两种价态Cu原子个数比2:1.
③Ba2+的配位数为10.
(1)A和B的单质单位质量的燃烧热大,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |

②根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为直线形.A原子杂化类型是sp.
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.
①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认识C60的熔点高于金刚石,你认为是否正确不正确理由是因为C60构成的晶体是分子晶体,影响分子晶体熔点的作用是分子间作用力;而金刚石构成的晶体是原子晶体,影响原子晶体熔点的作用是原子间共价键,共价键作用大大与分子间作用力,因此金刚石的熔点高于C60.
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.该物质的K原子和C60分子的个数比为3:1.晶胞中每个C60分子周围与之等距离且最近的C60分子数是6.
③继C60后,科学家又合成了Si60、N60;C、Si、N原子电负性由大到小的顺序是N>C>Si.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为30.
(3)1986年,瑞士两位科学家发现一种性能良好的金属氧化物超导体,使超导工作取得突破性进展,为此两位科学家获得了1987年的Nobel物理学奖.其晶胞结构如图3.
①根据图示晶胞结构,推算晶体中Y、Cu、Ba和O原子个数比,其化学式YBa2Cu3O7.
②已知该化合物中各元素的化合价Y为+3价,Ba为+2价,Cu为+2价和Cu为+3价,根据①所推出的化合物的组成,试计算化合物中这两种价态Cu原子个数比2:1.
③Ba2+的配位数为10.
10.下列物质属于天然高分子化合物的是( )
| A. | 油脂 | B. | 合成橡胶 | C. | 聚乙烯 | D. | 蛋白质 |
20.下列物质是烷烃的是( )
| A. | CH2Br-CH2Br | B. | C5H11OH | C. | C200H402 | D. | C6H6 |
 反应类型取代反应
反应类型取代反应