题目内容
7.A、B、C、D、E五种物质转化关系如图所示:
(1)A、B、D各为什么物质(填化学式):
ACu BCuCl2 DCu(OH)2
(2)写出下列过程的方程式(是离子反应的只写离子方程式):
A→B:Cu+Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$CuCl2
C→A:Fe+Cu2+=Fe2++Cu
D→E:Cu(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O.
分析 单质A与氯气加热反应发出棕色烟生成B,B溶于水呈得到绿色溶液C,则A为Cu、B为CuCl2;CuCl2与Fe反应生成Cu(A);C与NaOH溶液反应生成D[Cu(OH)2]沉淀,加热Cu(OH)2生成E(CuO),用氢气可将CuO还原成Cu,据此进行解答.
解答 解:(1)根据分析可知,A为Cu,B为CuCl2,D为Cu(OH)2,
故答案为:Cu;CuCl2;Cu(OH)2;
(2)A→B为Cu与氯气反应生成氯化铜,反应方程式为:Cu+Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$CuCl2 ;
C→A为Fe与氯化铜反应生成氯化亚铁和铜,反应方程式为:Fe+Cu2+=Fe2++Cu;
D→E为氢氧化铜分解生成氧化铜和水,反应方程式为:Cu(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O,
故答案为:Cu+Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$CuCl2 ;Fe+Cu2+=Fe2++Cu;Cu(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O.
点评 本题考查无机推断,题目难度不大,推断物质名称为解答结构,注意掌握常见元素及其化合物性质,试题侧重基础知识的考查,有利于提高学生的分析能力及逻辑推理能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| B. | 常温常压下,22.4LCO2和SO2混合气体含有2NA个O原子 | |
| C. | 常温常压下,8gCH4含有5NA个电子 | |
| D. | 1mol/LNaCl溶液中含有NA个Na+ |
15.单质钛的机械强度高,抗腐蚀能力强,有“未来金属”之称.工业上常用硫酸分解钦铁矿(主要成分是钛酸亚锈FeTiO3)的方法来制取TiO2,再由TiO2制金属钛.主要反应有:
①FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O
②Ti(SO4)2+3H2O=H2TiO3↓+2H2SO4
③H2TiO3$\frac{\underline{\;\;△\;\;}}{\;}$TiO2+H2O
④TiO2+2C+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4+2CO
⑤TiCl4+2Mg$\frac{\underline{\;\;△\;\;}}{\;}$2MgCl2+Ti.
下列叙述错误是( )
①FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O
②Ti(SO4)2+3H2O=H2TiO3↓+2H2SO4
③H2TiO3$\frac{\underline{\;\;△\;\;}}{\;}$TiO2+H2O
④TiO2+2C+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4+2CO
⑤TiCl4+2Mg$\frac{\underline{\;\;△\;\;}}{\;}$2MgCl2+Ti.
下列叙述错误是( )
| A. | 反应①属于非氧化还原反应 | |
| B. | 反应②属于非氧化迩原友应 | |
| C. | 反应④中TiO2是氧化剂 | |
| D. | 反应⑤表现了金属镁还原性比进士钛强 |
2.在天平两端的烧杯中,分别盛有足量等质量、等质量分数的稀硫酸,天平平衡后,往天平两端的烧杯中,分别加入等质量的镁和铜、铝合金,恰好完全反应,且天平仍保持平衡,则铜、铝合金中铜和铝的质量比为( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 2:1 |
12.下列物质中,既含有离子键,又含极性共价键的是( )
| A. | K2S | B. | NH4Cl | C. | Al2O3 | D. | Na2O2 |
19.某烃的结构简式为 ,它可能具有的性质是( )
,它可能具有的性质是( )
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 不易溶于水,易溶于苯等有机溶剂 | B. | 是芳香烃,也是苯的同系物 | ||
| C. | 能发生聚合反应,其产物可表示为 | D. | 分子中所有碳原子一定在同一平面 |
16.下列说法不正确的是( )
| A. | 常温下,在pH=6的硫酸铝溶液中,由水电离出的c(OH-)=10-6mol/L | |
| B. | 浓度为0.1mol•L-1的NaHCO3溶液:c(H2CO3)>c(CO32-) | |
| C. | 25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同 | |
| D. | 向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
8.下列实验室除杂所用试剂和操作均合理的为( )
| 选项 | 物质(括号中为杂质) | 除杂试剂 | 操作 |
| A | 碳酸钡(硫酸钡) | 饱和碳酸钠溶液 | 搅拌、过滤 |
| B | CO2(HCl) | 饱和碳酸钠溶液 | 洗气 |
| C | FeCl3(FeCl2) | 足量铁粉 | 搅拌、过滤 |
| D | HCl(Cl2) | 饱和食盐水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
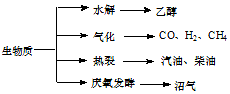 生物质资源是一种污染小的可再生能源,生物质的主要转化途径及主要产物如图.
生物质资源是一种污染小的可再生能源,生物质的主要转化途径及主要产物如图.