题目内容
5.关于非金属元素N、O、Cl、S的叙述,正确的是( )| A. | 在通常情况下其单质均为气体 | B. | 其单质均由双原子分子构成 | ||
| C. | 其单质都能跟某些金属单质反应 | D. | 每种元素仅生成一种氢化物 |
分析 A.S单质在通常状况下是固体;
B.臭氧为三原子分子,硫有S8等单质;
C.其单质都具有氧化性,能和某些金属单质反应;
D.O、N元素有多种氢化物.
解答 解:A.S单质在通常状况下是固体,其余元素单质在通常状况下是气体,故A错误;
B.臭氧为三原子分子,硫有S8等单质,所以其单质不一定是双原子分子,故B错误;
C.其单质都具有氧化性,能和某些金属单质反应,如:铁等金属能在氯气中燃烧,铁、铜能和S反应,故C正确;
D.O、N元素有多种氢化物,有O元素氢化物有水、双氧水,N元素氢化物有氨气、肼,故D错误;
故选C.
点评 本题考查非金属性元素及其化合物的性质,为高频考点,明确常见元素化合物结构、性质即可解答,注意N元素氢化物还有肼,为易错点.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
19.对于可逆反应,2SO2 (g)+O2(g)?2SO3(g)△H<0在一定温度下其平衡数为K,下列说法正确的是( )
| A. | 增大SO2的转化率K值一定增大 | B. | 减小压强K值减小 | ||
| C. | K值越大SO2转化率越大 | D. | 升高温度K值增大 |
17.有三种化合物:①NaHCO3、②Al(OH)3、③H2NCH2COOH,跟盐酸和氢氧化钠溶液都能反应的是( )
| A. | 只有② | B. | 只有①② | C. | 只有②③ | D. | ①②③ |
4.下列4种有机化合物中,能够发生酯化、加成和氧化3种反应是( )
| A. | CH2=CHCOOH | B. | CH2=CHCOOCH3 | C. | CH2=CHCH2OH | D. | CH3CH2CH2OH |
10.最近日本科学家确认世界还存在着另一种“分子足球”N60,它与C60分子结构相似.N60在高温和撞击后会释放出巨大能量.下列对N60的说法不正确的是( )
| A. | N60和14N都是氮的同位素 | B. | N60和N2都是氮的同素异形体 | ||
| C. | N60中氮原子之间由共价键结合 | D. | N60高温和撞击后应该生成N2 |
17.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.0L1.0mol•L-1的NaClO水溶液中含有的氧原子数为NA | |
| B. | 总质量为ag的CO和N2的混合物中所含原子总数为$\frac{a{N}_{A}}{14}$ | |
| C. | 2.24L 的2H35Cl分子中的中子数是1.9NA | |
| D. | 某密闭容器中盛有0.1mol N2和0.3molH2,在一定条件下充分反应,形成N-H键的数目为0.6NA |
14.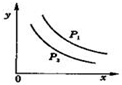 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )| A. | 上述正反应是放热反应 | B. | 上述正反应是吸热反应 | ||
| C. | 增大L的量,平衡正向移动 | D. | a<b |
15.用1L 1.0mol•L-1NaOH溶液吸收0.8molSO2,所得溶液中的SO32-和HSO3-的物质的量浓度之比是( )
| A. | 1:3 | B. | 1:2 | C. | 2:3 | D. | 3:2 |