��Ŀ����
����Ŀ��ͼ��һѧ����Ƶ���ʵ������ȡ�����������������ʵ��װ��ͼ�� 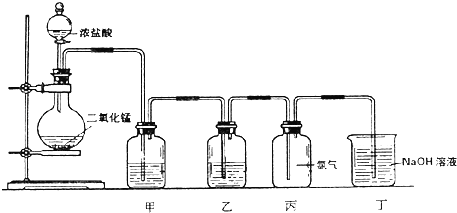
��1����ʵ��װ���л�ȱ�ٵ���������Ʒ���� ��
��2��Ϊ��ȥCl2�л��е�ˮ�������Ȼ������壬ϴ��ƿ�����зֱ�ʢ������������Һ������ţ����� �� �� A��ŨH2SO4 B������ʳ��ˮ C������ʯ��ˮ D������KI��Һ
��3����װ�õ������� �� ��Ӧ�����ӷ���ʽ�� ��
��4����ƿ�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��5����Ҫ���鼯��ƿ����ƿ�����Ƿ��ܷ�ã�����ʪ��ĵ��۵⻯����ֽ���м�⣬��©������ֽ��ɫ����Ӧ�����ӷ���ʽ�� ��
���𰸡�
��1���ƾ��ƣ�ʯ����
��2��B��A
��3������β������ֹ��Ⱦ��Cl2+2OH��=Cl��+ClO��+H2O
��4��MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
��5������Cl2+2I���T2Cl��+I2
���������⣺��1������������Ũ���ᷴӦҪ���ȣ���Ҫ�ƾ��ƣ���ƿ����Ҫ��ʯ���������Դ��ǣ��ƾ��ƣ�ʯ��������2�����ɵ������к����Ȼ����ˮ������ͨ��װ�ü������Ȼ��⣬ѡ��ʳ��ˮ��ͨ��װ��������ˮ������ѡ��Ũ���ᣬ���Դ��ǣ�B��A����3�������ж������ŷŵ������У���Ҫ������������Һ���գ���Ӧ�����ӷ���ʽΪ��Cl2+2OH��=Cl��+ClO��+H2O�����Դ��ǣ�����β������ֹ��Ⱦ��Cl2+2OH��=Cl��+ClO��+H2O����4������������Ũ�����ڼ��ȵ������������Ȼ��̡�������ˮ����ѧ��Ӧ����ʽΪ��MnO2+4HCl ��Ũ�� ![]() MnCl2+Cl2��+2H2O����5�����ܷⲻ�ã�������⻯�ط�Ӧ���ɵⵥ�ʣ���Ӧ���ӷ���ʽΪ��Cl2+2I���T2Cl��+I2 �� �ⵥ�������۱��������Դ��ǣ�����Cl2+2I���T2Cl��+I2 ��
MnCl2+Cl2��+2H2O����5�����ܷⲻ�ã�������⻯�ط�Ӧ���ɵⵥ�ʣ���Ӧ���ӷ���ʽΪ��Cl2+2I���T2Cl��+I2 �� �ⵥ�������۱��������Դ��ǣ�����Cl2+2I���T2Cl��+I2 ��
�����㾫����������Ĺؼ���������������ʵ�����Ʒ������֪ʶ������ʵ�����Ʒ���MnO2+4HCl��Ũ��=MnCl2+Cl2��+2H2O��

 Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�