题目内容
12.某烃可以用通式CnH2n来表示,下列有关此烃的说法正确的是( )| A. | 分子中有C=C双键 | B. | 分子中没有C=C双键 | ||
| C. | 分子可能有C=C双键 | D. | 分子中可能只含单键 |
分析 通式为C nH 2n的烃类可能是环烷烃,也可能为烯烃,据此解题.
解答 解:通式为C nH 2n的烃类可能是环烷烃,也可能为烯烃,可能含有C=C双键,也可能只含单键,故答案为:CD.
点评 本题考查了烃的通式,中等难度,解题关键看通式代表的是否只有一类物质.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
3.从实验室加热KClO3与MnO2的混合物制氧气后的剩余固体物中回收MnO2的操作顺序正确的是( )
| A. | 溶解、过滤、蒸发、洗涤 | B. | 溶解、蒸发、洗涤、过滤 | ||
| C. | 溶解、过滤、洗涤、干燥 | D. | 溶解、洗涤、过滤、干燥 |
7.下列有机反应中,都属于取代反应的是( )
| A. | 苯、乙烯分别使溴水褪色 | |
| B. | 溴乙烷分别在NaOH的水溶液、NaOH的醇溶液中反应 | |
| C. | 乙烯、甲苯使酸性KMnO4溶液褪色 | |
| D. | 苯、甲苯在一定条件下与混酸反应 |
4.既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有的乙烯的方法是( )
| A. | 在导管口处点燃 | B. | 通入足量高锰酸钾溶液中 | ||
| C. | 通入足量溴水中 | D. | 在一定条件下与H2反应 |
1.如图所示装置中,发生反应的离子方程式为Cu+2H+═Cu2++H2↑,下列说法正确的是( )


| A. | a、b不可能是同种材料的电极 | |
| B. | 该装置可能是电解池,电解质溶液为稀H2SO4 | |
| C. | 该装置可能是原电池,电解质溶液为稀HNO3 | |
| D. | 反应一段时间后,断开电路,向溶液中通入H2可使溶液复原 |
2.下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如表所示
请回答:(1)反应 ②是放热(填“吸热”或“放热”)反应.
(2)根据反应 ①与 ②可推导出K1、K2与K3之间的关系,则K3=$\frac{K{\;}_{2}}{K{\;}_{1}}$(用K1、K2表示).
(3)反应 ③能进行的主要原因是该反应是放热反应.
(4)反应 ①达到平衡时再加入少量铁粉,平衡将不移动(填“正向移动”、“不移动”或“逆向移动”);铁的转化率将减小(填“增大”、“不变”或“减小”).
(5)要使反应 ③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有BD.
A.缩小反应容器的容积 B.升高温度
C.使用合适的催化剂 D.设法减少平衡体系中的CO的浓度
(6)若反应 ③的逆反应速率与时间的关系如图所示:
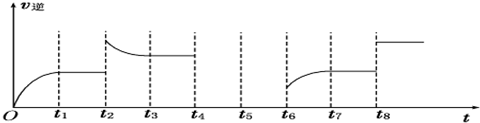
①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时增大生成物的浓度; t8时增大压强或使用催化剂.
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O(g)?CO2(g)+H2(g) | K3 | ? | ? |
(2)根据反应 ①与 ②可推导出K1、K2与K3之间的关系,则K3=$\frac{K{\;}_{2}}{K{\;}_{1}}$(用K1、K2表示).
(3)反应 ③能进行的主要原因是该反应是放热反应.
(4)反应 ①达到平衡时再加入少量铁粉,平衡将不移动(填“正向移动”、“不移动”或“逆向移动”);铁的转化率将减小(填“增大”、“不变”或“减小”).
(5)要使反应 ③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有BD.
A.缩小反应容器的容积 B.升高温度
C.使用合适的催化剂 D.设法减少平衡体系中的CO的浓度
(6)若反应 ③的逆反应速率与时间的关系如图所示:

①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时增大生成物的浓度; t8时增大压强或使用催化剂.



 .问:
.问: