题目内容
(10分)联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N2O4反应能放出大量的热。
(1)已知:2NO2(g)=====N2O4(g) △H=-57.20kJ?mol-1。一定温度下,在密闭容器中反应
2NO2(g)![]() N2O4(g)达到平衡。
N2O4(g)达到平衡。
其他条件不变时,下列措施能提高NO2转化率的是 (填字幕)
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量。则反应2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)的△H= kJ?mol-1
(3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300 mol?L-1、c(N2O4)=0.0120 mol?L-1。计算反应2NO2(g)![]() N2O4(g)的平衡常数K。
N2O4(g)的平衡常数K。
(4)现用一定量的Cu与足量的浓HNO3反应,制得1.00L已达到平衡的N2H4和NO2的混合气体(17℃、1.01×105Pa),理论上至少需消耗Cu多少克?
(1)BC
![]() (2)-1224.96
(2)-1224.96
![]() (3)根据题意知平衡时:
(3)根据题意知平衡时:![]() ;
; ![]()
K=![]()
答:平衡常数为13.3。
(4)由(3)可知,在17℃、1.01×105Pa达到平衡时,1.00L混合气体中:
![]()
![]()
则![]()
由![]() ===
===![]() 可得
可得
![]()
答:理论上至少需消耗Cu 1.73 g.
【解析】(1)考查影响化学平衡移动的因素(2)简单的反应热计算要注意将质量转化为物质的量,还要注意比例关系。(3)(4)见答案

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
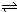 N2O4(g)达到平衡.
N2O4(g)达到平衡.