题目内容
联氨(N2H4)及其衍生物是一类重要的火箭燃料,N2H4与N2O4反应能放出大量的热.(1)已知:2NO2(g)?N2O4(g)△H=-57.20KJ?mol-1.一定温度下,在密闭容器中反应2NO2(g)?N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是 (填字母)
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量.写出该反应的热化学方程式 .
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量.写出该反应的热化学方程式
分析:(1)该反应是反应前后气体体积减小的、放热的可逆反应,要提高二氧化氮的转化率,只要改变条件使化学平衡向正反应方向移动即可,依据平衡移动原理分析选项;
(2)依据题干数据计算2mol肼完全燃烧放热,结合热化学方程式书写方法标注物质聚集状态,和对应焓变来解答.
(2)依据题干数据计算2mol肼完全燃烧放热,结合热化学方程式书写方法标注物质聚集状态,和对应焓变来解答.
解答:解:(1)该反应是反应前后气体体积减小的、放热的可逆反应,要使该反应向正反应方向移动,可改变反应物的浓度、体系的压强、温度等,
A、减小N02的浓度,平衡向逆反应方向移动,N02的转化率降低,故A错误;
B.降低温度,平衡向正反应方向移动,N02的转化率提高,故B正确;
C.增加N02的浓度,相当于体系压强增大,利于反应向正反应方向移动,N02的转化率提高,故C正确;
D.升高温度,平衡向逆反应方向移动,N02的转化率降低,故D错误;
故答案为:BC;
(2)1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量,则2molN2O4(l)的质量为2mol×32g/mol=64g,放出热量为19.14kJ×64=1224.96KJ的热量,反应的热化学方程式为:2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1224.96KJ/mol,
故答案为:2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1224.96KJ/mol.
A、减小N02的浓度,平衡向逆反应方向移动,N02的转化率降低,故A错误;
B.降低温度,平衡向正反应方向移动,N02的转化率提高,故B正确;
C.增加N02的浓度,相当于体系压强增大,利于反应向正反应方向移动,N02的转化率提高,故C正确;
D.升高温度,平衡向逆反应方向移动,N02的转化率降低,故D错误;
故答案为:BC;
(2)1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量,则2molN2O4(l)的质量为2mol×32g/mol=64g,放出热量为19.14kJ×64=1224.96KJ的热量,反应的热化学方程式为:2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1224.96KJ/mol,
故答案为:2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1224.96KJ/mol.
点评:本题考查化学平衡计算、反应热计算、影响化学平衡因素分析判断,掌握基础是解题关键,难度中等.

练习册系列答案
相关题目
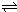 N2O4(g)达到平衡.
N2O4(g)达到平衡.