��Ŀ����
��һ���¶��£���2molSO2��1molO2ͨ��һ���ݻ��ɱ���ܱ�������������·�Ӧ�� 2SO2��g��+O2��g�� 2SO3��g�������˷�Ӧ���е�һ���̶�ʱ���ﵽ��ѧƽ��״̬����ά���¶Ȳ��䣬��a��b��c�ֱ������ʼ�����SO2��O2��SO3�����ʵ�����ʹ�ôﵽƽ��ʱ��Ӧ������������������������Ը�����ƽ��ʱ����ȫ��ͬ������д���пհף�
2SO3��g�������˷�Ӧ���е�һ���̶�ʱ���ﵽ��ѧƽ��״̬����ά���¶Ȳ��䣬��a��b��c�ֱ������ʼ�����SO2��O2��SO3�����ʵ�����ʹ�ôﵽƽ��ʱ��Ӧ������������������������Ը�����ƽ��ʱ����ȫ��ͬ������д���пհף���1����a=0��b=0����c�ķ�ΧΪ______ ��
��2����a=0.5����b=______��c�ķ�ΧΪ______��
��3��a��b��c���������һ��������__________��
��1����0
��2��0.25����0
��3��a=2b��a��0��c��0����a��c��ͬʱΪ0
�����������
��һ���¶ȡ������ݻ��ɱ䡱���¶ȡ�ѹǿһ�����Ҧ�n��g����0�������������ɣ���֪��ʱ�γɵĵ�Чƽ���ǵȱ�ƽ�⡣���ü�ֵ�����㡣
��1��a=0��b=0ʱ����Ӧ���淴Ӧ����ʼ����ʱ���ۼ���SO3�����ʵ���Ϊ���٣����ü�ֵ���������Կ����������ʵ���֮��Ϊ2��1�����SO2��O2����������ʼ̬��Ӧ�ɱ��������cֻҪ�������0���ɡ�
��2�����ü�ֵ�����ɵȱ�ƽ��Ĺ��ɿ�֪��SO2�����ʵ���aΪ0.5mol��O2һ��Ҫ�������ʵ���bΪ0.25mol��SO3�����ʵ���ֻҪ����c��0������ɱ�����������
��3�� 2SO2��g�� + O2��g��
 2SO3��g��
2SO3��g��n��ʼ��0��mol�� 2 1 0
n��ʼ��1��mol�� a b c
n��ʼ��2��mol�� a+c b+0.5c 0
��Ϊ��ʱ�γɵĵ�Чƽ���ǵȱ�ƽ�⣬���ԣ�a+c���ã�b+0.5c��=2��1����ã�a=2b��a��0��c��0����a��c��ͬʱΪ0��

��ϰ��ϵ�д�
�����Ŀ
 ����һ���¶��£���2mol N2��6mol H2ͨ��һ�����������ܱ������У���ͼ��������Ӧ��N2��g��+3H2��g��
����һ���¶��£���2mol N2��6mol H2ͨ��һ�����������ܱ������У���ͼ��������Ӧ��N2��g��+3H2��g�� 2NH3 ��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���û������Ϊ7mol���ݴ˻ش��������⣺
2NH3 ��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���û������Ϊ7mol���ݴ˻ش��������⣺
 2NH3 (g�� ������ӦΪ���ȷ�Ӧ��
2NH3 (g�� ������ӦΪ���ȷ�Ӧ�� 2NH3 ��g�� ������ӦΪ���ȷ�Ӧ��
2NH3 ��g�� ������ӦΪ���ȷ�Ӧ��

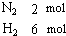
 2NH3 ��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���û������Ϊ7mol���ݴ˻ش��������⣺
2NH3 ��g��������ӦΪ���ȷ�Ӧ������Ӧ�ﵽƽ���û������Ϊ7mol���ݴ˻ش��������⣺ 2SO3��g������������Ҫ����д�հף�
2SO3��g������������Ҫ����д�հף�
