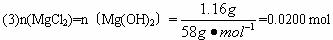题目内容
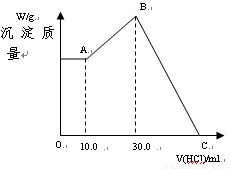
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的悬浊液中逐滴加入1 mol·L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.试完成下列问题:
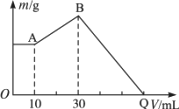
(1)A点沉淀物的化学式为________;B点沉淀物的化学式为________.
(2)原混合物中的MgCl2的物质的量为________,AlCl3的物质的量为________,NaOH的物质的量为________.
(3)HCl溶液在Q点的加入量是________.
解析:
答案:(1)Mg(OH)2 Mg(OH)2、Al(OH)3
(2)0.02 mol 0.02 mol 0.03 mol (3)130 mL
剖析:①盐酸加入量在0-10 mL时,沉淀的质量没有改变,说明未加盐酸时,沉淀物为Mg(OH)2,溶液为NaAlO2和NaOH的混合液,其过程中加盐酸是中和剩余混合物中的NaOH,A处的悬浊液为Mg(OH)2、NaAlO2、NaCl,则原混合物中n(MgCl2)=1.16 g/58 g·mol-1=0.02 mol.
②加入盐酸10-30 mL过程时,发生反应为:![]() +H++H2O
+H++H2O![]() Al(OH)3↓,B沉淀的化学式为Mg(OH)2、Al(OH)3,原溶液中n(AlCl3)=(30-10)×10-3 L×1 mol·L-1=0.02 mol,B点沉淀量达到最大值,其中溶液为NaCl溶液.所以n(NaOH)=n(HCl)=30×10-3 L×1 mol·L-1=0.03 mol.
Al(OH)3↓,B沉淀的化学式为Mg(OH)2、Al(OH)3,原溶液中n(AlCl3)=(30-10)×10-3 L×1 mol·L-1=0.02 mol,B点沉淀量达到最大值,其中溶液为NaCl溶液.所以n(NaOH)=n(HCl)=30×10-3 L×1 mol·L-1=0.03 mol.
③设Mg(OH)2、Al(OH)3完全溶解时,所消耗盐酸的体积为V mL,V×10-3 L×1 mol·L-1=0.02 mol×2+0.02 mol×3,V=100 mL,所以Q点表示加入了130 mL.

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案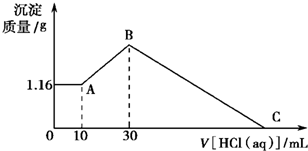 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:?
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:?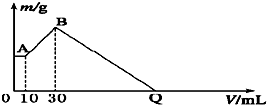 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答: