题目内容
下图为原电池的示意图。请回答:

(1)Zn极为原电池的 (填“正”或“负”)极,该极的电极反应式是 ,属于 (填“氧化反应”或“还原反应”)。
(2) (填“电子”或“电流”)从锌片通过导线流向铜片,溶液中的H+从 (填“锌片”或“铜片”)获得电子
【答案】
(1)负极;Zn-2e-=Zn2+ 氧化反应 (2)电子, 铜片
【解析】考查原电池的判断。在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。锌比铜活泼,所以锌是负极,失去电子。铜正极,溶液中的氢离子在正极得到电子,生成氢气。

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
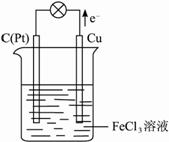



 的从
(填“锌片”或“铜片”)获得电子。
的从
(填“锌片”或“铜片”)获得电子。 溶液的浓度(填“增大”或“减小”,下同),烧杯中溶液的质量 。
溶液的浓度(填“增大”或“减小”,下同),烧杯中溶液的质量 。