题目内容
回答以下问题:
(1)Ni(CO)4是无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测Ni(CO)4是____________分子(填“极性”或“非极性”)。
| 共价键 | C-C | C-N | C-S |
| 键能/ kJ·mol-1 | 347 | 305 | 259 |
(2)已知:波长为300nm的紫外光的光子所具有的
能量约为399 kJ/mol。根据右表有关蛋白质分子中
重要化学键的信息,说明人体长时间照射紫外光后
皮肤易受伤害的原因:______________________________________________________________
_____________________________________________________________。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①N2H4分子中含有极性键的数目是___________ ;NH4+的空间构型是_______________。
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g) △H=-1038.7kJ·mol-1
若该反应中有8mol N-H键断裂,则形成的π键有________mol。
 (4)硼砂是含结晶水的四硼酸钠,其阴离子
(4)硼砂是含结晶水的四硼酸钠,其阴离子![]() (含B、O、H三种元素)的球棍模型如右图所示:
(含B、O、H三种元素)的球棍模型如右图所示:
①在![]() 中,硼原子轨道的杂化类型有 和________;配位键存在于 原子之间(填原子的数字标号);m= (填数字)。
中,硼原子轨道的杂化类型有 和________;配位键存在于 原子之间(填原子的数字标号);m= (填数字)。
②硼砂晶体由![]() 、
、![]() 和
和![]() 构成,它们之间存在的作用力有 (填序号)。
构成,它们之间存在的作用力有 (填序号)。
A.共价键 B.离子键 C. 氢键 D.范德华力 E. 金属键
(1)非极性(1分)
(2)紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子(2分) ks5u
(3)①4 (1分) 正四面体 (1分) ks5u
② 6mol(1分) ks5u
(4)①SP2杂化 (1分) SP3杂化(1分) 4、5(1分),m=2(1分) ②B C D(2分,漏选得1分,有错选不得分)





 +RX
+RX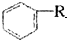 +HX(R.是烃基,X为卤原子)
+HX(R.是烃基,X为卤原子)