题目内容
(2011?安庆三模)A、B、C、D、E为原子序数依次增大的短周期元素,其相关信息如下表:
请回答:
(1)E原子的核外电子排布式是
(2)比较顺序:第一电离能:C
(3)E的单质与Z反应,生成的由三种元素组成的化合物的电子式为: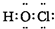
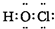 ;D和E的电负性的大小为:D
;D和E的电负性的大小为:D
(4)A、C、E三种元素形成的一种化合物的水溶液呈酸性,该化合物的晶体类型是
(5)B与D一般情况下可形成两种常见气态化合物,若存在一种直线型气态化合物B2D2分子,且各原子最外层都满足8电子结构,则B2D2可能的结构简式为
(6)写出一个常见的Y→Z转化的化学反应方程式
| 元素 | 相关信息 |
| A | A能分别与B、C、D形成电子总数相等的分子X、Y、Z |
| B | B基态原子的价电子结构为nsnnpn |
| C | D与B在同一周期,D原子核外未成对电子数等于电子层数 |
| D | E的最高价氧化物的水化物是酸性最强的含氧酸 |
(1)E原子的核外电子排布式是
1s22s22p63s23p5(或[Ne]3s23p5)
1s22s22p63s23p5(或[Ne]3s23p5)
.(2)比较顺序:第一电离能:C
>
>
D,键长:A-C>
>
A-D(填“>”、“<”或“=”).(3)E的单质与Z反应,生成的由三种元素组成的化合物的电子式为:
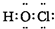
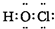
>
>
E(填“>”、“<”或“=”).(4)A、C、E三种元素形成的一种化合物的水溶液呈酸性,该化合物的晶体类型是
离子
离子
(填“分子”、“原子”或“离子”)晶体,晶体中的化学键类型有共价键、离子键
共价键、离子键
(填“离子键”或“共价键”).(5)B与D一般情况下可形成两种常见气态化合物,若存在一种直线型气态化合物B2D2分子,且各原子最外层都满足8电子结构,则B2D2可能的结构简式为
O=C=C=O
O=C=C=O
.(6)写出一个常见的Y→Z转化的化学反应方程式
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
分析:B基态原子的价电子结构为nsnnpn,n应为2,则B的原子序数为6,应为C元素,D与B在同一周期,D原子核外未成对电子数等于电子层数,则D的核外电子排布式为1s22s22p4,应为O元素,B、C、D原子序数依次增大,则C为N元素,A能分别与B、C、D形成电子总数相等的分子X、Y、Z,则A为H元素,X、Y、Z分别为CH4、NH3、H2O,E的最高价氧化物的水化物是酸性最强的含氧酸,应为Cl元素,对应的含氧酸为HClO4,结合元素对应原子的结构、单质和化合物的性质可解答该题.
解答:解:B基态原子的价电子结构为nsnnpn,n应为2,则B的原子序数为6,应为C元素,D与B在同一周期,D原子核外未成对电子数等于电子层数,则D的核外电子排布式为1s22s22p4,应为O元素,B、C、D原子序数依次增大,则C为N元素,A能分别与B、C、D形成电子总数相等的分子X、Y、Z,则A为H元素,X、Y、Z分别为CH4、NH3、H2O,E的最高价氧化物的水化物是酸性最强的含氧酸,应为Cl元素,则
(1)E为Cl,原子序数为17,核外电子排布式为1s22s22p63s23p5(或[Ne]3s23p5),
故答案为:1s22s22p63s23p5(或[Ne]3s23p5);
(2)N元素的2p轨道为半充满状态性质稳定,难以失去电子,则第一电离能大于O,
N原子半径大于O原子半径,则键长N-H>O-H,
故答案为:>;>;
(3)Cl2与H2O反应生成HCl和HClO,HClO为三种元素组成的化合物,为共价化合物,电子式为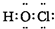 ,
,
O的电负性为3.5,Cl的电负性为3.0,则电负性O>Cl,
故答案为: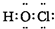 ;>;
;>;
(4)H、N、Cl三种元素形成的一种化合物为NH4Cl,水解呈酸性,为离子化合物,含有离子键和共价键,
故答案为:离子;共价键、离子键;
(5)B为C,D为O,一种直线型气态化合物C2O2分子,且各原子最外层都满足8电子结构,则C和O之间为C=O,C和C之间为C=C,结构式为O=C=C=O,
故答案为:O=C=C=O;
(6)NH3在催化条件下可与O2反应生成NO和H2O,反应的化学方程式为4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O.
(1)E为Cl,原子序数为17,核外电子排布式为1s22s22p63s23p5(或[Ne]3s23p5),
故答案为:1s22s22p63s23p5(或[Ne]3s23p5);
(2)N元素的2p轨道为半充满状态性质稳定,难以失去电子,则第一电离能大于O,
N原子半径大于O原子半径,则键长N-H>O-H,
故答案为:>;>;
(3)Cl2与H2O反应生成HCl和HClO,HClO为三种元素组成的化合物,为共价化合物,电子式为
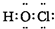 ,
,O的电负性为3.5,Cl的电负性为3.0,则电负性O>Cl,
故答案为:
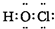 ;>;
;>;(4)H、N、Cl三种元素形成的一种化合物为NH4Cl,水解呈酸性,为离子化合物,含有离子键和共价键,
故答案为:离子;共价键、离子键;
(5)B为C,D为O,一种直线型气态化合物C2O2分子,且各原子最外层都满足8电子结构,则C和O之间为C=O,C和C之间为C=C,结构式为O=C=C=O,
故答案为:O=C=C=O;
(6)NH3在催化条件下可与O2反应生成NO和H2O,反应的化学方程式为4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
点评:本题考查原子结构与元素周期律知识,题目难度中等,本题侧重于物质结构的考查,为该题的难点,也是易错点,原子的结构特征是推断元素的种类常考查的角度,学习中注意相关知识的积累.

练习册系列答案
相关题目
 (2011?安庆三模)竖炉冶铁工艺流程如图所示,燃烧室中主要反应为:
(2011?安庆三模)竖炉冶铁工艺流程如图所示,燃烧室中主要反应为: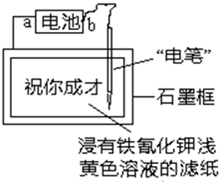 (2011?安庆三模)已知:含Fe2+的溶液与铁氰化钾K3[Fe(CN)6]溶液反应生成具有特征蓝色的铁氰化亚铁沉淀.现用如图装置在浸有铁氰化钾浅黄色溶液的滤纸上写出特征蓝色的字“祝你成才”.据此判断下列说法正确的是( )
(2011?安庆三模)已知:含Fe2+的溶液与铁氰化钾K3[Fe(CN)6]溶液反应生成具有特征蓝色的铁氰化亚铁沉淀.现用如图装置在浸有铁氰化钾浅黄色溶液的滤纸上写出特征蓝色的字“祝你成才”.据此判断下列说法正确的是( )