��Ŀ����
��13�֣�ijʵ��С������ͼ��ʾװ�ý���ͭ��Ũ���ᷴӦ��ʵ��̽����
(1)д�����з�Ӧ�Ļ�ѧ����ʽ�� ��
(2)���Թܿڵ���Ӧմ�е��Լ��� ���������� ��
(3)ʵ��С���Ա�۲����Թ���Һ��仯�� ��
(4)��ַ�Ӧ�������Թ�����ͭƬʣ�࣬��������м���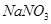 ��Һ������ͭƬ�ܽ⣬�˷�Ӧ�����ӷ���ʽΪ ��
��Һ������ͭƬ�ܽ⣬�˷�Ӧ�����ӷ���ʽΪ ��
(5)��100mL 18mol��L-1��Ũ�����м��������ͭƬ������ʹ֮��ַ�Ӧ�������������ڱ�״���µ���������� ��(����ĸ)
A��40.32L B��30.24L C��20.16L D��13.44L
��13�֣�
��1��Cu+2H2SO4 CuSO4+SO2��+2H2O��2�֣�
CuSO4+SO2��+2H2O��2�֣�
��2��NaOH��Һ�������������𰸣���2�֣�������δ��Ӧ��SO2����ֹ��Ⱦ��������2�֣�
��3��Ʒ����Һ��ɫ��2�֣�
��4��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��2�֣�
��5��D��3�֣�
����:

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д����ᣨH2C2O4����һ����Ҫ�Ļ���ԭ�ϡ���֪������0��01 mol��L-l��H2C2O4��KHC2O4��K2C2O4��Һ��pH���±���ʾ��
|
| H2C2O4 | KHC2O4 | K2C2O4 |
| pH | 2��0 | 3��1 | 8��1 �� |
��1����������������ʱ�����д�ʩ��ʹKHC2O4��Һ��c��K+����c��HC2O4-���ӽ�1��1����_________������ĸ����
A������������H2C2O4 B������������KHC2O4
C������������Na2C2O4 D��������Һ���¶�
��2��ȡһ������H2C2O4��2H2O��KHC2O4�Ļ�����ˮ�ܽ⣬���250 mL��Һ��ȡ���ݴ���Һ��25 mL�����һ����Һ���ȼ��뼸�η�̪��Һ���ٵμ�0��25 mol��L-l NaOH��Һ��20��00 mLʱ����Һ����ɫ��Ϊdz��ɫ����ڶ�����Һ�еμ�����3 mol��L-l H2S04��Һ�ữ����0��10 mol��L-lKMnO4��Һ�ζ���������KMnO4��Һ16��00 mLʱ����Һ����ɫ��Ϊdz�Ϻ�ɫ����ش��������⣺
��������ӷ���ʽ��5C2O42-+2MnO4-+16H+��10______+2Mn2++8H2O��
��ԭ�������H2C2O4��2H2O��KHC2O4�����ʵ���֮��Ϊ__________��
��3��ijʵ��С������ͼ��ʾ��װ��̽��FeC2O4��2H2O�ڸ����������������ȷֽ�IJ����36��0g FeC2O4��2H2O��ַ�Ӧ������������Ϊ13��6g��Ũ��������7��2g����ʯ������11��0g�����������ijɷֺ����ʵ���������֪FeC2O4��2H2O����Է�������Ϊ180���跴Ӧ���������屻������գ�

 ʵ���⣺ijʵ��С������ͼ��ʾװ�ý���ͭ��Ũ���ᷴӦ��ʵ��̽����
ʵ���⣺ijʵ��С������ͼ��ʾװ�ý���ͭ��Ũ���ᷴӦ��ʵ��̽����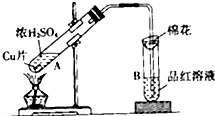 ijʵ��С������ͼ��ʾװ�ý���ͭ��Ũ���ᷴӦ��ʵ��̽����
ijʵ��С������ͼ��ʾװ�ý���ͭ��Ũ���ᷴӦ��ʵ��̽����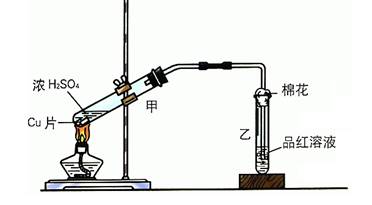
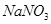 ��Һ������ͭƬ�ܽ⣬�˷�Ӧ�����ӷ���ʽΪ
��
��Һ������ͭƬ�ܽ⣬�˷�Ӧ�����ӷ���ʽΪ
��