题目内容
下列对价电子构型为2s22p5的元素描述正确的是( )
分析:价电子构型为2s22p5的元素为F元素,位于第二周期第ⅤⅡA族,结合元素的位置及性质来解答.
解答:解:价电子构型为2s22p5的元素为F元素,位于第二周期第ⅤⅡA族,
A.同周期中原子半径最小为F,周期表中原子半径最小的为H,故A错误;
B.F的原子序数为9,故B正确;
C.在第二周期中从左向右第一电离能增大,但N原子的最外层p电子半满,为稳定结构,第一电离能大于F,故C错误;
D.F的非金属性最强,其电负性最大,故D正确;
故选BD.
A.同周期中原子半径最小为F,周期表中原子半径最小的为H,故A错误;
B.F的原子序数为9,故B正确;
C.在第二周期中从左向右第一电离能增大,但N原子的最外层p电子半满,为稳定结构,第一电离能大于F,故C错误;
D.F的非金属性最强,其电负性最大,故D正确;
故选BD.
点评:本题考查核外电子排布,利用价电子排布推出元素是解答本题的关键,注意结合元素周期律来解答,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 ,A原子的最外层电子数等于其电子层数。D和E可以形成原子个数比为1:1和1:2的两种离子化合物,且D原子的2p能级上有两个未成对电子,试回答下列问题:
,A原子的最外层电子数等于其电子层数。D和E可以形成原子个数比为1:1和1:2的两种离子化合物,且D原子的2p能级上有两个未成对电子,试回答下列问题: 学式,下同);第一电离能从大到小的顺序是
学式,下同);第一电离能从大到小的顺序是  _____________,D2-的结构示意图___________。A、D可形成多种化合物,其中一种是氧化剂,其水溶液有弱酸性,写出该化合物的结构式________________,分子中含有_____________________键(填“极性”或“非极性”,下同)是__________分子。
_____________,D2-的结构示意图___________。A、D可形成多种化合物,其中一种是氧化剂,其水溶液有弱酸性,写出该化合物的结构式________________,分子中含有_____________________键(填“极性”或“非极性”,下同)是__________分子。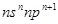 ,A原子的最外层电子数等于其电子层数。D和E可以形成原子个数比为1:1和1:2的两种离子化合物,且D原子的2p能级上有两个未成对电子,试回答下列问题:
,A原子的最外层电子数等于其电子层数。D和E可以形成原子个数比为1:1和1:2的两种离子化合物,且D原子的2p能级上有两个未成对电子,试回答下列问题: