题目内容
下列实验操作中不正确的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口处 |
| C、蒸发时,要用玻璃棒不断搅动溶液 |
| D、过滤时,将待过滤的液体直接倒入漏斗,使液面低于滤纸的边缘 |
考点:过滤、分离与注入溶液的仪器,蒸发和结晶、重结晶,蒸馏与分馏,分液和萃取
专题:
分析:A.分液时注意防止液体污染;
B.温度计测量蒸气的温度;
C.蒸发应防止局部受热不均匀;
D.转移液体需要引流.
B.温度计测量蒸气的温度;
C.蒸发应防止局部受热不均匀;
D.转移液体需要引流.
解答:
解:A.为防止液体污染,分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒,故A正确;
B.蒸馏操作时,温度计水银球应靠近蒸馏烧瓶的支管口处,故B正确;
C.蒸发应防止局部受热不均匀,则用玻璃棒不断搅动,使受热均匀,不会导致液滴飞溅,故C正确;
D.转移液体需要用玻璃棒引流,故D错误.
故选D.
B.蒸馏操作时,温度计水银球应靠近蒸馏烧瓶的支管口处,故B正确;
C.蒸发应防止局部受热不均匀,则用玻璃棒不断搅动,使受热均匀,不会导致液滴飞溅,故C正确;
D.转移液体需要用玻璃棒引流,故D错误.
故选D.
点评:本题考查物质的分离提纯实验操作,为高频考点,把握混合物分离操作中的注意事项为解答的关键,侧重实验基本技能的考查,题目难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
下列溶液与100mL0.5mol/LNa2SO4溶液中的 Na+的物质的量浓度相等的是( )
| A、200mL0.5mol/LNaCl溶液 |
| B、100mL1mol/LNa2CO3溶液 |
| C、100mL0.5mol/LNa3PO4溶液 |
| D、1L1mol/LNaOH溶液 |
下列实验中,所选装置或实验设计合理的是( )


| A、用图①和②所示装置进行粗盐提纯 |
| B、用乙醇提取溴水中的溴选择图③所示装置 |
| C、用图④所示装置进行稀盐酸浓缩得到浓盐酸 |
| D、图⑤所示装置中盛有饱和Na2SO3溶液除去SO2中含有的少量HCl |
氮氧化铝(AlON)属原子晶体,是一种超强透明材料,可以由反应Al2O3+C+N2
2AlON+CO合成,下列有关说法正确的是( )
| ||
| A、氮氧化铝中氮的化合价是-3 |
| B、AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同 |
| C、反应中每生成5.7gAlON同时生成1.12LCO |
| D、反应中氧化产物和还原产物的物质的量之比是2:1 |
下列离子方程式中错误的是( )
| A、明矾净水的原理:Al3++3H2O=Al(OH)3↓+3H+ |
| B、硫酸铝溶液与硫化钠溶液混合:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑ |
| C、碳酸钠溶液呈碱性的原因:CO32-+2H2O?H2CO3+2OH- |
| D、FeCl3溶液加入碳酸氢钠溶液中:Fe3++3HCO3-=Fe(OH)3↓+3CO2↑ |
下列离子方程式中,正确的是( )
| A、稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| B、氧化镁与稀盐酸混合:MgO+2H+═Mg2++H2O |
| C、碳酸钡与盐酸:CO32-+2H+═H2O+CO2↑ |
| D、Ba(OH)2加入H2SO4:Ba2++SO42-═BaSO4↓ |
某常见有机物(一个分子内碳原子总数不超过10个)的结构简式可表示为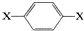 ,其核磁共振氢谱图中出现两组峰,且不同化学环境的氢原子数之比为3:2.下列关于该有机物的说法错误的是( )
,其核磁共振氢谱图中出现两组峰,且不同化学环境的氢原子数之比为3:2.下列关于该有机物的说法错误的是( )
 ,其核磁共振氢谱图中出现两组峰,且不同化学环境的氢原子数之比为3:2.下列关于该有机物的说法错误的是( )
,其核磁共振氢谱图中出现两组峰,且不同化学环境的氢原子数之比为3:2.下列关于该有机物的说法错误的是( )| A、该有机物不可能为芳香醇 |
| B、该有机物的分子式可能为C8H10O2 |
| C、该有机物可能与NaOH溶液反应 |
| D、该有机物可能与溴水反应 |
下列过程一定不能自发发生的是( )
| A、水从高处流向低处 |
| B、食盐溶解于水中 |
| C、水分解成H2和O2 |
| D、生石灰与水反应生成熟石灰 |
关于分散系,下列叙述中正确的是( )
| A、分散系分为胶体和溶液 |
| B、电泳现象可证明胶体带电荷 |
| C、利用丁达尔效应可以区别溶液与胶体 |
| D、按照分散质和分散剂状态不同(固、液、气),它们之间可有6种组合方式 |