题目内容
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH =+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
根据上述反应,下列说法正确的是
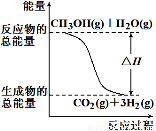
A.反应①中的能量变化如图所示
B.可推知2H2(g)+O2(g)=2H2O(g) ?ΔH=-483.8 kJ/mol
C.1 mol CH3OH充分燃烧放出的热量为192.9 kJ
D.CH3OH转变成H2的过程一定要吸收能量
B
【解析】
试题分析:反应①中生成物的总能量大于反应物的总能量,故A错误;根据盖斯定律,(②-①)×2得,2H2(g)+O2(g)=2H2O(g) ΔH=-483.8 kJ/mol,故B正确;CH3OH充分燃烧,生成二氧化碳和水,故C错误;反应②放热,故D错误。
考点:本题考查化学反应与能量。

练习册系列答案
相关题目