题目内容
本题16分,①下列两幅谱图是结构简式为CH3CH2CH2OH和CH3CH(OH)CH3的两种有机化合物的1H核磁共振谱图。请判断哪一幅是CH3CH(OH)CH3的1H—NMR谱图,并说明理由。(6分)

②、0.2 mol有机物和0.4 mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。燃烧后的这些产物经过浓H2SO4后,质量增加10.8 g;再通过灼热的CuO充分反应后,固体质量减轻3.2 g,最后气体再通过碱石灰被完全吸收,质量增加17.6 g。(可能用到的相对原子质量H-1,C-12,O-16,Cu-64)
(1)推断该有机物的分子式。(6分)
(2)若0.2 mol该有机物在与过量的金属钠完全反应后放出4.48 L H2(标准状况),试确定有机物的结构简式。(4分)?
①A(3分) 理由:从结构上分析,CH3CH(OH)CH3有三种不同化学环境的H,而CH3CH2CH2OH有四种不同的H,故从图上分析,A上有三个峰,而B有四个峰,故A是CH3CH(OH)CH3的1H—NMR谱图(3分)。
②(1)浓硫酸增加的质量就是水的质量,所以水是10.8g,物质的量是0.6mol。CO通过灼热的氧化铜又被氧化生成CO2,所以有机物完全燃烧产生的CO2是17.6g,物质的量是0.4mol。根据方程式CO+CuO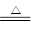 Cu+CO2可知,每消耗1molCO,固体质量就减少16g,所以CO的物质的量是3.2÷16=0.2mol。即有机物燃烧生成物是0.2CO2、0.2molCO和0.6mol水。所以根据原子守恒可知有机物中氧原子的物质的量是0.4mol+0.2mol+0.6mol-0.4mol×2=0.4mol,因此有机物的最简式为CH3O。因为2个碳原子最多结合6个氢原子,所以化合物的分子式为C2H6O2.
Cu+CO2可知,每消耗1molCO,固体质量就减少16g,所以CO的物质的量是3.2÷16=0.2mol。即有机物燃烧生成物是0.2CO2、0.2molCO和0.6mol水。所以根据原子守恒可知有机物中氧原子的物质的量是0.4mol+0.2mol+0.6mol-0.4mol×2=0.4mol,因此有机物的最简式为CH3O。因为2个碳原子最多结合6个氢原子,所以化合物的分子式为C2H6O2.
(2)标准状况下4.48L氢气的物质的量是0.2mol,因为2个羟基,生成1分子氢气,所以有机物中羟基的个数是2个,因此是乙二醇,结构简式为HOCH2CH2OH。
【解析】①考查有机物中氢原子种类的判断。首先同一个碳原子上的氢原子是相同的,其次同一个碳原子所连接的所有甲基上的氢原子是相同的,再就是具有对称性结构的(类似于平面镜成像中物体和像的关系)。所以CH3CH2CH2OH和CH3CH(OH)CH3中的氢原子种类分别是4和3种。即CH3CH(OH)CH3的1H—NMR谱图是A。
②考查有机物分子式及结构简式的判断。
(1)浓硫酸增加的质量就是水的质量,所以水是10.8g,物质的量是0.6mol。CO通过灼热的氧化铜又被氧化生成CO2,所以有机物完全燃烧产生的CO2是17.6g,物质的量是0.4mol。根据方程式CO+CuO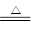 Cu+CO2可知,每消耗1molCO,固体质量就减少16g,所以CO的物质的量是3.2÷16=0.2mol。即有机物燃烧生成物是0.2CO2、0.2molCO和0.6mol水。所以根据原子守恒可知有机物中氧原子的物质的量是0.4mol+0.2mol+0.6mol-0.4mol×2=0.4mol,因此有机物的最简式为CH3O。因为2个碳原子最多结合6个氢原子,所以化合物的分子式为C2H6O2.
Cu+CO2可知,每消耗1molCO,固体质量就减少16g,所以CO的物质的量是3.2÷16=0.2mol。即有机物燃烧生成物是0.2CO2、0.2molCO和0.6mol水。所以根据原子守恒可知有机物中氧原子的物质的量是0.4mol+0.2mol+0.6mol-0.4mol×2=0.4mol,因此有机物的最简式为CH3O。因为2个碳原子最多结合6个氢原子,所以化合物的分子式为C2H6O2.
(2)标准状况下4.48L氢气的物质的量是0.2mol,因为2个羟基,生成1分子氢气,所以有机物中羟基的个数是2个,因此是乙二醇,结构简式为HOCH2CH2OH。


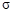 键与
键与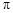 键的个数比为
键的个数比为 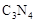 形成的原子晶体,结构类似
形成的原子晶体,结构类似
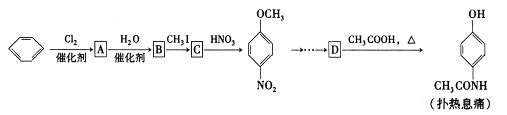
 C的反应类型为 ,D中官能团的名称为 。
C的反应类型为 ,D中官能团的名称为 。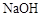 溶液反应,理论上消耗
溶液反应,理论上消耗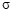 键与
键与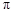 键的个数比为
键的个数比为 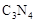 形成的原子晶体,结构类似
形成的原子晶体,结构类似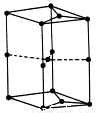

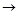 C的反应类型为 ,D中官能团的名称为 。
C的反应类型为 ,D中官能团的名称为 。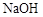 溶液反应,理论上消耗
溶液反应,理论上消耗