题目内容
7.某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验.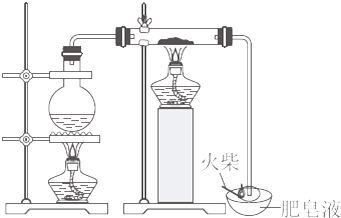
(1)用如图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水反应).反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当肥皂泡破裂,产生爆鸣声(填实验现象)时,说明“铁与水蒸气”能够进行反应.写出铁与水反应的化学方程式3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2
(2)为了证明反应后的固体混合物中含有+3价的Fe,他们计划取出少量混合物于试管中,加入足量的盐酸,溶解、过滤.写出有关的化学方程式Fe3O4+8HCl═FeCl2+2FeCl3+4H2O.
分析 (1)根据铁与水蒸气在高温下反应生成四氧化三铁和氢气,氢气点燃有爆鸣声进行分析;
(2)根据四氧化三铁与盐酸反应生成氯化亚铁、氯化铁、水写出方程式.
解答 解:(1)铁与水蒸气在高温下反应生成四氧化三铁和氢气,3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2; 如果肥皂泡破裂,产生爆鸣声说明有氢气生成,即可说明“铁与水蒸气”能够进行反应,
故答案为:肥皂泡破裂,产生爆鸣声;3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(2)四氧化三铁与盐酸反应生成氯化亚铁、氯化铁、水,所以方程式为:Fe3O4+8HCl═FeCl2+2FeCl3+4H2O,
故答案为:Fe3O4+8HCl═FeCl2+2FeCl3+4H2O.
点评 本题考查铁与水蒸气反应方程式的书写,氢气的检验方法,以及金属氧化物与盐酸反应生成对应的盐和水的知识,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.若NA代表阿伏加德罗常数,下列表述正确的是( )
| A. | 标准状况下,11.2L NH3中含共价键的数目为1.5NA | |
| B. | 均含NA个氧原子的氧气和臭氧的质量比为3:2 | |
| C. | 1.8克D2O中含有NA个中子 | |
| D. | 过氧化钠与水反应转移NA个电子时,产生氧气的体积在标准状况下为11.2L |
7.如图为冰的一种骨架形式,依此为单位向空间延伸,请问该冰中的每个水分子有几个氢键( )

| A. | 2 | B. | 4 | C. | 8 | D. | 12 |
12. 如图,对10mL一定物质的量浓度的盐酸用一定物质的量浓度的NaOH溶液滴定的图象,可推出盐酸和NaOH溶液的物质的量浓度是表内各组中的( )
如图,对10mL一定物质的量浓度的盐酸用一定物质的量浓度的NaOH溶液滴定的图象,可推出盐酸和NaOH溶液的物质的量浓度是表内各组中的( )
 如图,对10mL一定物质的量浓度的盐酸用一定物质的量浓度的NaOH溶液滴定的图象,可推出盐酸和NaOH溶液的物质的量浓度是表内各组中的( )
如图,对10mL一定物质的量浓度的盐酸用一定物质的量浓度的NaOH溶液滴定的图象,可推出盐酸和NaOH溶液的物质的量浓度是表内各组中的( )| A | B | C | D | |
| c(HCl)/mol•L-1 | 0.12 | 0.04 | 0.03 | 0.09 |
| c(NaOH)/mol•L-1 | 0.04 | 0.12 | 0.09 | 0.03 |
| A. | A | B. | B | C. | C | D. | D |
 乙二醛电解氧化制备乙醛酸(OHC-COOH)的生产装置如图所示,通电后,阳极产生的Cl2与乙二醛溶液反应生成乙醛酸.
乙二醛电解氧化制备乙醛酸(OHC-COOH)的生产装置如图所示,通电后,阳极产生的Cl2与乙二醛溶液反应生成乙醛酸.